美国疾控中心(CDC)国家环境卫生中心(NCEH)前主任,美国有毒物质和疾病登记局(ATSDR)前主任Portier博士2017年向法庭提交的草甘膦除草剂致癌性《专家意见》
【编译者说明:
1)“草甘膦除草剂致癌性”问题首先一个科学问题,必须由与草甘膦及其捆绑转基因产业毫无利益关系的独立科学家通过科学、客观、严谨科学实验与流行病学研究研究来评断,而不能由已经堕落为草甘膦及其捆绑转基因产业利益共同体者评断!
2)任何国家监管机构或国际组织监管机构,过去一旦渎职犯罪批准或支持草甘膦除草剂继续“农药登记”,它们就堕落与草甘膦及其捆绑转基因产业形成利益共同体,丧失了对草甘膦除草剂安全性评价的科学、客观、公正性,而且无法自拔解套!
3)美国疾控中心(CDC)国家环境卫生中心(NCEH)前主任,美国有毒物质和疾病登记局(ATSDR)前主任Portier博士,是该领域难得的有良知权威人士。2017年他向美国法庭提交的《专家意见》,对于“草甘膦致癌性”问题提交了最全面、最科学、客观、公正的证据链,值得中国毒理学工作者认真研读!
4)该《专家意见》非常详尽篇幅很长(原文供97页),本文仅节录其中“资质”、评估资料、“因果关系评估方法”,及其“草甘膦致癌性”关键性证据汇总部分。读者如果希望审查《专家意见》中对每篇研究文献的评述,建议访问本译文附录“证据”。
5)本文专业性非常强,建议一般读者仅阅读最前边的“资质”、“信赖清单”(评估的文献种类)与“因果关系评估方法”部分。
6)建议医学院校在校学生、医学工作者、毒理学专业人士,流行病学专业人士阅读内容更详尽的本译文附录“证据”全文。】
2017年10月,美国草甘膦除草剂致淋巴癌诉讼证词:Christopher J. Portier博士对于草甘膦除草剂致癌性向法庭提交的《专家意见》(案件3:16-md-02741 -VC 文件654-17,注册日期:2017年10月28日,共97页)
资质
我于1977年从(路易斯安那州)尼科尔斯州立大学(Nicholls State University)获得了数学学士学位,并在北卡罗来纳大学公共卫生学院分别于1979年和1981年获得生物统计学硕士学位与博士学位。我的博士学位论文探讨了设计一项为期两年的啮齿类动物致癌性研究的最佳方法,以评估一种化学品引起癌症的能力[1,2]。 大多数研究人员仍使用我论文中的最佳剂量模式。
我获得博士学位后的第一份工作是在美国环境健康科学研究所(NIEHS)和美国国家毒理学计划(NTP)的联合任命下,进行毒理学中通常使用的实验的设计和分析研究。
在NIEHS / NTP工作的32年中,我参与了我个人研究活动之外的许多国家优先事项。... 在NIEHS / NTP期间,我还担任与我的资格相关的行政职务。从2000年到2006年,我担任NIEHS的环境毒理学计划(ETP)主任。
我于2010年离开NIEHS/NTP,出任美国疾病控制与预防中心(CDC)的国家环境卫生中心(NCEH)的主任,同时担任有毒物质和疾病登记局(ATSDR)的主任。 NCEH进行研究并支持旨在减少环境危害对公共卫生的影响的活动。NCEH的一项备受推崇的研究工作是国家生物监测计划。该程序测试在美国全国人群中人体血液和尿液中是否存在数百种化学物质。
除了我在联邦工作中的职务外,我还担任过许多国家和国际科学咨询小组的成员。就本声明的资格而言,最值得注意的是,2005年至2010年期间我担任总统国家科学技术委员会毒理和风险小组委员会的主席,1998年至2003年期间担任美国环保署(EPA)科学顾问小组的成员和主席(特别关注关于为农药计划提供咨询的建议),同时担任国际癌症研究机构(IARC)咨询小组主席,该小组更新并改进了其审查科学数据的规则,以确保关于人体暴露致癌性的结论是最佳的(序言)[30]。...
我发表过250多篇关于毒理学与风险评估方面经同行审查的论文、专著章节与技术文件。...
我为美国环保署(EPA),美国食品和药物管理局(FDA),美国疾病控制与预防中心(CDC),国立卫生研究院(NIH),世界卫生组织(WHO)和国际癌症研究机构(IARC)的风险评估做出了贡献。
信赖清单
在准备本报告的过程中,我查看了以下材料:
a. 所有有关草甘膦制剂引起人类非霍金斯淋巴瘤(NHL)能力的流行病学数据。
b. 关于非霍金斯淋巴瘤(NHL)细胞起源的科学论文
c. 与草甘膦引起的致癌性,遗传毒性和氧化应激有关的同行评审科学数据
d. 被告向原告律师提供的有关草甘膦致癌性的技术报告
e.美国环保署(EPA)、欧洲食品安全机构(EFSA)、德国联邦风险评估研究所、欧洲化学机构、国际癌症研究机构(IARC)和世卫组织(WHO)/粮农组织(FAO)农药残留联席会议对与农药残留有关的科学文献审查草甘膦可能致癌的文件。
f. 欧洲食品安全机构(EFSA)提供的有关被告以外的组织准备的有关草甘膦的动物致癌性数据的技术文件
g. 诉讼中产生的其他各种文件
本报告结尾列出我依赖的文件的完整清单。
因果关系评估方法
草甘膦和/或草甘膦制剂(GBF)是否会引起人类非霍金斯淋巴瘤(NHL)的评估需要对人类研究(流行病学)、动物癌症研究以及研究化学物质导致癌症的机制进行研究的科学证据进行回顾和综合。许多不同的方法[31,32]用于综合这三个科学领域,以回答“这种化学物质是否会导致人类癌症?”的问题。在这三个科学领域中,任何一个领域必须对单个研究的质量进行评估和总结,以确保整体评估中所包括的研究适当完成。一旦评估了各个研究的质量,就需要对研究支持人类癌症发现的程度做出判断。为此,美国环保署(EPA),国际癌症研究机构(IARC),欧洲化学局(EChA),美国致癌物报告以及许多其他人使用的准则[30, 33-35]依赖于Hill(1965)[36]制定的“因果关系标准的方面”。
Hill列出了在评估因果关系时应考虑的流行病学研究和相关科学的九(9)个方面。这些方面中的任何一个的存在与否都不足以得出因果关系的推论。相反,这九个方面是回答其他解释是否比因果推断更可信的问题的手段。希尔指出:
“我的九种观点中,没有一种能够为因果假设提供支持或反对的无可争辩的证据,而且没有必要作为正当条件。它们或多或少可以做的事情是帮助我们对这个基本问题下定决心-- 是否有其他方法可以解释我们面前的那组事实,是否有其他相同或更多的答案,是更可能的原因与结果?”
Hill引用的9个方面包括:1) 观察到的关联的一致性,2) 观察到的关联的强度,3) 生物学上的合理性,4) 生物学梯度,5) 观察到的关联的时间关系,6) 观察到的关联的特异性,7) 连贯性,8) 来自人类实验和9) 类比的证据。这些将在下面简要描述。
当几项研究表明癌症与暴露之间存在一致的正相关性时,就可以加强因果关系的推断。这解决了重复研究的关键问题,这在大多数科学辩论中都至关重要。如果研究不一致,则应考虑研究质量、潜在混淆、潜在偏倚和统计功效方面的差异,以更好地理解这种不一致。
当在几项研究中观察到的关联的强度大且精确时,就可以加强因果关系的推断。这些大而精确的关联减少了观察到的关联是由于偶然或偏见而产生的可能性。患癌症的风险略有增加并不能排除因果关系,因为诸如效力和暴露水平之类的问题可能会降低研究识别更大风险的能力。荟萃分析对一些风险较小的研究进行了客观评估,以帮助阐明所观察到的关联强度。
当有证据支持通过实验证据证明的生物合理性时,因果关系的推论得到加强。动物致癌性研究(在评估暴露于纯草甘膦的实验动物中的肿瘤发生率)在建立生物学合理性中起着重要作用。可能导致癌症的机制类型很多[37],其中大多数可以通过在动物、人类细胞、动物细胞和/或其他实验系统中进行的实验研究来证明。偶尔,职业、意外或意外的人类接触使研究人员可以使用直接的人类证据来评估机制。
当存在生物学梯度显示暴露随变化而变化的合理风险模式时(例如,风险随着暴露增加或暴露时间延长而增加),则因果关系的推论得到加强。在许多流行病学研究中,由于研究设计的局限性或结果的表述不够清晰,无法对此方面进行检查。当研究确实解决了暴露-反应关系时,未能找到关系可能是由于暴露范围小,样本量不足或暴露量随时间变化而未考虑在内。
当存在暴露于癌症之前的时间关系时,因果关系的推论得到加强。这是显示因果关系所必需的。如果不存在,则不存在因果推论。由于癌症的潜伏期可能长(年),因此研究评估应考虑暴露时间是否足够长,才与癌症发展相关。
当暴露特定于给定的癌症时,因果关系的推论得到加强。这意味着正在研究的疾病终点仅是由于所评估的原因。这个问题很少适用,并且由于非霍金斯淋巴瘤(NHL)还有其他原因,因此特异性不适用于草甘膦的因果关系确定。
当其他实验证据与流行病学证据中所见关联的因果解释有一贯性时,就可以加强因果关系的推断。为了评估一贯性,将考虑来自动物致癌性研究、机理研究以及所研究化学物质代谢信息的信息。
在人类中有实验证据支持因果解释时,因果关系的推论得到加强。解决化学品的毒性时,很少有可用的此类信息。但是,在个人评估中减少或限制暴露量并降低癌症风险的实验将对评估产生重大影响(例如,评估与继续吸烟相比停止吸烟的人的癌症风险的研究表明,肺癌风险降低了)。没有可用的草甘膦此类数据。
最后,当存在其他具有类似性结构的化学试剂在人和/或动物中表现出相似的作用和/或在机理研究中显示出相似的生物学影响时,因果关系的推论得到加强。没有可用的草甘膦此类数据。
推论因果关系的最合乎逻辑的方法是逐步骤研究Hill (1965)[36]提出的因果关系的各个方面,并将其应用于草甘膦和草甘膦制剂的可用数据。这在以下各节中完成。
在人类流行病学研究中所见关联的一贯性
相关流行病学研究
【注:对每篇研究文献的评述在此从略,如果希望审查,请访问本译文附录的“证据”】
Chang and Delzell (2016)[38]... Cantor et al. (1992)[39]...De Roos et al. (2003)[43]... Zahm et al. (1990)[51]... Hoar et al. (1986)[52]...Lee et al. (2004)[44]...Nordstrom et al. (1998)[40]...Hardell and Eriksson (1999)[41]...Hardell et al. (2002)[42]通过结合Nordstrom et al. (1998)[40]与Hardell and Eriksson (1999)[41]... Hardell et al. (2002)...Eriksson et al. (2008)[46]... McDuffie et al. (2001)[50]... Hoar et al. (1986)[52]... Zahm et al. (1990)[51]...Hohenadel et al. (2011)[48]... McDuffie et al. (2001)[50]... Chang and Delzell (2016)[38]...Orsi et al. (2009)[47]... Cocco et al. (2013)[49]... De Roos et al. (2005)[45]...
关联一贯性
Hill (1965)[36]将一致性定义为对“是否由不同的人在不同的地点、环境和时间反复观察到这个问题”的回答“是”。对于这些研究,答案的确是肯定的。
如果草甘膦与非霍金斯淋巴瘤(NHL)关联的人群相对危险度(PRR)等于1(无作用),则可以预期多项研究中的统计学显着性结果极少,并且约有一半的研究的OR或RR均低于1一半以上。正如国际癌致研究机构(IARC)专著112( IARC Monograph 112, 2015)[56]和Chang and Delzell (2016)[38]所指出的,在比较研究时,最合理的比较是使用调整最充分的风险估计。我主要将我的评论仅限于这些经过最充分调整的风险估算。
多个流行病学研究之间的关联一贯性不仅是查看有多少统计学意义上的显着性,还有不是显着的,还必须解决响应方向的一贯性。图1显示了先前讨论的流行病学研究中所有OR和RR的森林图。森林图中的每条水平线均以黑色正方形表示OR / RR的平均估计值,并且随着晶须从黑色正方形向左和向右延伸,该估计值周围的95%置信区间为该值。
从图1得出的第一个显而易见的结论是,所有平均OR / RR估计值(黑色正方形)始终≥1。这意味着所有的研究都朝着积极的方向发展。在他们的荟萃分析中,Schinasi and Leon (2014)[57],IARC (2015)[56]以及Chang and Delzell (2016)[38]均将6篇论文(图1中以红色突出显示)确定为评估草甘膦诱导人产生NHL的能力最可靠的论文:McDuffie et al. (2001)[50],Hardell et al. (2002)[42],De Roos et al. (2003)[43]和De Roos et al. (2005)[45],Eriksson et al. (2008)[46]和Orsi et al. (2009)[47]。我将这些论文称为六种流行病学核心研究。如上所述,如果真实的潜在风险比率为1(无影响),则您会期望约一半的发现低于1,一半等于1或更大。仅使用6个核心研究的结果,您会发现所有≥1;发生这种情况的可能性为(0.5)6或0.016,强烈表明研究与潜在的PRR = 1不符,并且它们始终支持阳性的作用。
评估一贯性的第二种方法是使用荟萃分析将各个研究合并,以使用OR和RR(CRR)进行合并分析,并检验研究中的异质性。Chang and Delzell (2016)进行的荟萃分析与IARC (2015)进行的分析相同,是对Schinasi and Leon (2014)的改进,因此,我将集中讨论使用Chang and Delzell (2016)荟萃分析。Chang and Delzell (2016)使用两种不同的方法(随机效应模型和固定效应模型)对草甘膦流行病学研究进行了四个单独的荟萃分析。在他们的第一个分析(模型1)5中,他们结合了六项核心研究中经过最充分调整的风险估计,得出随机效应模型和固定效应模型的CRR为1.27(1.01-1.59),从而支持了在这些研究中接触非霍金斯淋巴瘤(NHL)和草甘膦相关。在第二种分析(模型2)中,它们逻辑回归分析的结果,随机效应模型和固定效应模型的CRR为1.30(1.03-1.64)替代了De Roos et al. (2003)的贝叶斯分析结果。在第三次分析(模型3)中,他们从模型1中用他们从来自Hohenadel et al. (2011)的分析合并的荟萃分析结果(该研究重新分析了与McDuffie et al. (2001)相同的数据,将哮喘患者和非哮喘患者之间的结果进行了划分)替代了McDuffie et al. (2001)的结果,对随机效应模型和固定效应模型得出CRR为1.32(1.00-1.73)的结果。最后,在第四种分析(模型4)中,他们使用模型3,用通过logistic回归分析得出的结果取代了De Roos et al. (2003)的贝叶斯分析,得出随机效应模型和固定效应模型的CRR为1.37(1.04-1.82)。从本质上讲,所有不同的荟萃分析均未拒绝组合的、统计学上显着的阳性影响的概念。
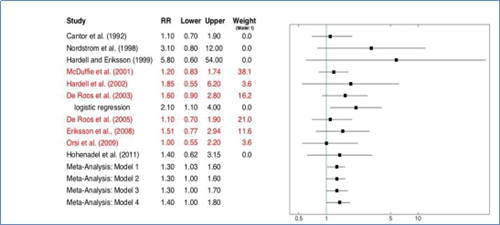
图1:来自某些流行病学研究和Chang and Delzell (2016)的荟萃分析中,经过最充分调整的风险估计的赔率和比率比率。 “ RR”是指研究中的OR或RR,“ Lower”是指95%的下限,“ Upper”是95%的上限,“ Weight”是指应用于模型1中特定研究的权重 荟萃分析(Chang and Delzell (2016)中的表3)。 对于De Roos et al. (2003),第一行用于贝叶斯模型分析,第二行标记为“逻辑回归”,来自逻辑模型分析。
如上所述,评估流行病学数据一贯性的另一种方法是评估研究的异质性。异质性可能是由于参与者、结果、暴露量度、对研究对象的质疑方法、对象性别等的差异所致。Chang and Delzell (2016)使用Cochran的Q统计量和C检验了六项核心研究结果的异质性。 I2统计信息[58]。对于模型1-4,来自Cochran Q检验的p值分别为0.84、0.59、0.85和0.63(通常,如果p <0.10,则您拒绝同质研究的概念,而支持异质研究)。所有四个模型的I2统计量均为0.0%(I2的值范围可以在0-100%之间,并且考虑到异质性高于50%)。固定效应模型和随机效应模型给出相同结果的事实也支持数据缺乏异质性。在这六项核心研究中没有迹象表明存在异质性。缺乏异质性支持对荟萃分析的解释,因为这表明在六项核心研究中发现存在正相关和强烈一贯性。
Chang and Delzell (2016)还在可能的情况下评估非霍金斯淋巴瘤(NHL)亚型与草甘膦暴露之间的关联。对于B细胞淋巴瘤,他们结合了Eriksson et al. (2008)[46]的结果和Cocco et al. (2013)[49]的研究,并看到CRR(随机效应和固定效应)为2.0(1.1-3.6),I2为0,Cochran Q检验p值为0.58。对于弥漫性大B细胞淋巴瘤,他们结合了Eriksson et al. (2008)[46]的结果和Orsi et al. (2009)[47]的研究,并看到CRR(随机效应和固定效应)为1.1(0.5-2.3),I2为0,Cochran Q检验p值为0.79。对于合并的慢性淋巴细胞性白血病和小淋巴细胞性淋巴瘤,他们将Eriksson et al. (2008)[46]的结果和Orsi et al. (2009)[47]的研究结合在一起,并看到CRR使用1.3(0.2-10)的随机效应模型和1.9(0.9-4.0)的固定效应模型,I2为83.7%,Cochran's Q检验p值为0.01。对于滤泡性淋巴瘤,他们结合了Eriksson et al. (2008)的结果[46]与Orsi et al. (2009)[47]的研究一样,并看到CRR(随机效应和固定效应)为1.7(0.7-3.9),I2为0,Cochran Q检验p值为0.73。最后,对于毛细胞白血病(HCL),他们结合了Nordstrom et al. (1998)[40]的结果和Orsi et al. (2009)[47]的研究,并看到CRR(随机效应和固定效应)为2.5(0.9-7.3),I2为0,Cochran Q检验p值为0.63。这些亚型分析基于少量病例,只有两项研究使它们在单独考虑时无法可靠地解决数据一致性问题。但是,将它们与NHL核心研究的荟萃分析结果相结合时,这些研究为这些数据一贯性的结论提供了支持。
Chang and Delzell (2016)也对仅具有相似特征的研究进行了荟萃分析,从而进行了敏感性分析。 使用仅五项病例对照研究,CRR为1.3(1.0-1.7)。将它们分为所使用的对照类型,使用的人口对照的四项研究CRR为1.4(1.0-1.8)。对仅男性的四项研究的CRR仅为1.3(1.0-1.7),对男性和女性的两项研究的CRR为1.2(0.8-1.8)。 在北美进行了三项研究,其CRR为1.2(1.0- 1.6),在欧洲进行了三项研究,其CRR为1.3(0.8-2.1)。 这三项研究中有两项在瑞典进行,其CRR为1.6(0.9-2.8)。 对于固定效应模型和随机效应模型,所有产生的主要CRR均相同。 该敏感性分析表明,六项核心研究相结合的结果与各自研究的主要CRR相比相差无几,这为不同研究中一贯性的发现增加了支持。
在案例对照研究中,当案例和对照选择参加研究的原因可能导致系统性偏见时,就会出现选择偏见,而这些偏见可能导致与所研究的暴露无关的阳性或阴性结果。例如,如果有暴露的病例比有暴露的对照更有可能参与,那么结果将是更高的OR值;但是,这种差异必须是差异性的,而不仅仅是参与率的差异。在其中的一些研究中,选择对照的方法可能会导致选择偏倚,从而导致OR升高。但是,鉴于五项核心病例对照研究中使用的病例和对照类型多种多样,这不太可能解释这些研究中发现的一贯性发现。如果未完成问卷/访谈的原因在病例和对照之间不同并且与暴露有关,则缺乏病例与对照的完整数据也可能导致选择偏倚。这些报告中没有迹象表明这种选择偏见,这不可能解释这些数据中的一致性。
在病例对照研究和队列研究中,暴露分类错误可导致OR或RR值增加或减少。 例如,在病例对照研究中,如果病例比对照更有可能说他们接触了草甘膦,则这会增加OR值;这是召回偏见的一种。在队列研究中这种类型的偏见可能性较小。 在所有六项核心研究中,作者都讨论了这个问题。在每种情况下,他们均得出结论,一定会有一些暴露分类错误,但很可能是非差异性的,这意味着错误分类是随机的; 这可能会减少研究中看到的OR / RR,而不是增加它们。
当存在与草甘膦接触和非霍金斯淋巴瘤(NHL)诊断密切相关的接触或某些其他因素从而造成混淆,如果能够加以控制,则可以解释结果。这些研究中最有可能引起混淆的原因是接触其他农药。六项核心研究中有四项[42, 43, 45, 46]控制了与其他农药的接触,并且发现的结果与其他两项研究基本相同。另一个令人困惑的问题是,这些病例是否存在与NHL相关的免疫缺陷;在所有病例对照研究中,此类病例均被排除在外。最后,其他农业暴露(例如动物、其他化学物质、传染原)可能与草甘膦暴露相关,并可能与NHL相关;没有一项研究能控制这些因素。但是,并非所有暴露的病例都是农民。如果通过其他农业暴露也造成混淆,则无法从这些数据确定这种影响的大小或方向。
总之,我们有四个不同的研究小组在两个不同的大陆上使用不同的设计、调查表和研究人群进行的六项核心流行病学研究,这些研究高度一致,没有明显的偏倚或不能解释结果的混淆。 六个核心研究之间的关联是一致的。
[50] McDuffie,H.H.,et al., Non-Hodgkin'slymphomaandspecificpesticide exposures in men:cross-Canadastudyof pesticidesand health. Cancer EpidemiolBiomarkersPrev,2001.10(11): p.1155-1163.
[42] Hardell,L.,M.Eriksson,andM. Nordstrom,Exposuretopesticidesasriskfactorfornon-Hodgkin'slymphomaandhairycellleukemia:pooledanalysisoftwoSwedishcase-controlstudies. Leuk.Lymphoma,2002.43(5):p.1043-1049.
[43] DeRoos,A.J.,et al.,Integrative assessmentofmultiplepesticidesasriskfactorsfornon-Hodgkin'slymphomaamongmen. OccupEnvironMed,2003.60(9): p.E11.
[45] De Roos,A.J.,etal.,Cancerincidenceamongglyphosate-exposedpesticideapplicatorsintheAgriculturalHealthStudy. EnvironHealthPerspect,2005.113(1):p.49-54.
[46] Eriksson,M.,etal.,Pesticideexposureasriskfactorfornon-Hodgkinlymphomaincludinghistopathologicalsubgroupanalysis. IntJCancer,2008.123(7):p.
[47] Orsi,L.,etal.,Occupationalexposuretopesticidesandlymphoidneoplasmsamongmen:resultsofaFrenchcase-controlstudy. OccupEnvironMed,2009.66(5): p.291-8.
这六项核心流行病学研究,所有研究均显示(草甘膦与非霍金森淋巴瘤之间关联)优势比(OR)/相对危险度(RR)大致相同,适度增加,如果组合起来,则显示出显着的关联强度。六个核心研究之间有着很强的联系。
确定草甘膦与非霍金森淋巴瘤之间关联因果关系的汇总分析方法
在来自不同实验室对同一实验动物模型进行多种致癌性研究是不寻常的。科学文献中也没有描述对多种动物癌症生物测定的组合分析方法。但是,如流行病学[92,93]中所进行的汇总分析方法也可用于组合动物致癌性研究。基本概念是将来自相同性别/物种/品系的所有数据汇总到一项研究中并进行适当分析。基本步骤是:1)选择要汇总的研究;2)合并数据进行分析;3)评估研究的具体效果;4)估计合并效应;5)解释合并效应与个别效应之间的差异;6)尽可能进行敏感性分析。这些步骤将用于分析动物致癌性研究的汇总数据,其中按性别、物种、品系和暴露时间进行汇总,以限制汇总研究中异质性。《联邦杀虫、杀菌和灭鼠法》(FIFRA)科学咨询小组在针对环保署(EPA)的草甘膦致癌性问题向EPA提出的建议中[54],强烈支持引用我对EPA的评论[94],使用汇总分析来解决一致性问题。
Lankas et al. (1981)[74]的研究中,50只雄性与50只雌性SD大鼠接触于饲料中草甘膦(98.7%纯度)26个月(参考表1看剂量)。
这个研究与OECD(经济合作与发展组织)指导原则不一致(从事该项研究时在OECD指导原则发布前),但是,如同EFSA(欧洲食品安全机构)[89]注明的那样,该项研究与OECD1981年指导原则大体一致。对于该项研究的信息可以从美国环保署(EPA)[61]、EFSA[89]、Greim et al.[91]获得,以及由Bio/dynamics Inc.实验室做的原研究报告[95]以及孟山提供给EPA的备忘录获得。
在雌鼠中观察到甲状腺C-cell癌增加(pTrend=0.003)(表1),但是将腺瘤和癌合并在一起只是略微增加(pTrend=0.072)。孟山都邀请来的独立毒理学家争辩说这些肿瘤没有进行相关处理。作者提供了癌症和癌的联合来自九个对照组的腺瘤的历史对照数据,对于癌的平均反应为4/453 = 0.9%,对于联合肿瘤为46/453 = 10.2%。 使用历史控制数据,两个结果的统计学意义都没有改变。
作者们还提到胸腺和淋巴结中淋巴细胞增生的发生率略高于对照组(p趋势=0.143)。中间剂量组与对照显著区别(pFisher=0.018)。
这项研究中还发现胰岛细胞瘤在最低剂量组雄鼠中统计显著增加(pFisher=0.028)(表1),但是在其他剂量组没有这种情况;趋势测试不显著(p趋势=0.312)。
这项研究SD大鼠中用的最高剂量远低于MTD(最大容忍剂量)。尽管欧洲食品安全机构(EFSA)[89]注明这项研究大体符合OECD(经济合作与发展组织)指导原则,然而,他们由于使用的低剂量的情况认为它不符合现行的指导方针而将其驳回。EPA[61]也将这项研究排除在考虑之外。然而,该研究发现的男性睾丸肿瘤和女性甲状腺C细胞癌增加,有必要仔细评估确定因果关系。此外,这是最长时间(26个月)的研究,为整体评估提供了独特的信息。
表1中其他研究使用SD大鼠也见到显著增加的其他肿瘤也列出来。
表1:Lankas (1981)[74]26个月喂养研究雄性与雌性SD大鼠中令人关注的肿瘤
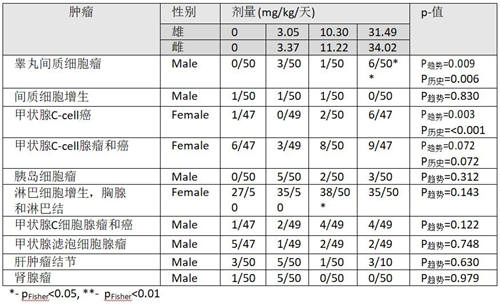
总之,本研究显示雄性SD大鼠睾丸间质细胞瘤和肝细胞腺瘤的阳性结果,以及雌性SD大鼠甲状腺c细胞癌的阳性反应,将纳入对(草甘膦-致癌)因果关系的整体评估。
Stout and Ruecker (1990)[78]研究中,50只SD雄鼠与50只SD雌鼠接触于饲料中草甘膦24个月(具体剂量间表2)。这项研究依照OECD(经济合作与发展组织)指导原则进行。
该研究中没观察到存活差别,也没有表明使用的最高剂量超过了最高容忍剂量。
在所有剂量组中,相对于雄性大鼠对照组,胰岛细胞肿瘤增加,并且对于最低(pFisher = 0.015)和最高(pFisher = 0.032)剂量组(表2)统计学显着。但是,这些比率包括一年中处死的10只动物。在一年内终止的大鼠,由于接触时间短,可能没有发生这种肿瘤的风险;将一年处死的这些动物包括在最终肿瘤计数中是非常罕见的(EPA [61]也排除了这些动物)。在本研究的病理学表中,在临时处死的10只动物中没有任何肿瘤。去除这10只动物不会改变趋势或Fisher精确检验的p值。该实验室中该肿瘤的历史对照数据报告为23/432或5.3%[96],与该控制率的趋势比较并不显著(p历史t = 0.15)。这种趋势的缺乏由回应的上下性质驱动。假设5.3%的历史比率正确,那么在47只动物中发现8个或更多肿瘤的概率是0.003。与此类似,对于中剂量和高剂量,这个概率分别为0.124和0.014。雌性没有表现出这种肿瘤增加。作者提供了一个表,其中包含自该研究的胰岛 - 细胞腺瘤和癌的以及来自Lankas等人(1981)[74]研究的肿瘤计数合并结果,作者们争辩认为这样的结果不显示与剂量相关的增加。喂养26个月研究的动物与喂养24个月研究的动物对相同化学物质和非常不同的对照发病率可能具有非常不同的反应。
在雄性大鼠中,除去中期处死的动物后,肝细胞腺瘤有统计学显著性趋势(p趋势= 0.015),腺瘤和癌合并有显著增加(p趋势 = 0.05,表2),但雌鼠没显示(未显示)。 肝癌通常也在单独的分析中提供,但这些数据不是作者提供的(数据表明肝细胞癌将具有负面趋势)。
无论是否包括临时处死动物(表2),雌性大鼠甲状腺C细胞腺瘤也显着增加(p趋势 = 0.049),而且腺瘤和癌合在一起未边际增加6(p趋势 = 0.052)。 在雄性中,腺瘤趋势为p趋势 = 0.084,对于腺瘤和癌一起p趋势 = 0.091。 在中期处死雄性大鼠中观察到腺瘤,表明中期处死雄性大鼠时处于该肿瘤风险中。如果将这些动物重新添加到分析中,则雄性趋势测试对于腺瘤为p趋势 = 0.063,对于腺瘤和癌合并在一起为p趋势 = 0.068。
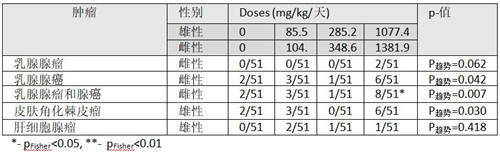
其他SD鼠喂养研究中显示显著的其他几种肿瘤也包括在表2中,它们在本研究中没有显示显著作用。
作为结论,这项研究中发现胰岛细胞瘤发病率增加,不能作为偶然发现轻易排除。 发现雄性大鼠肝腺瘤显著增加而癌未增加的结果到可能是偶然的。应该将雄性和雌性鼠甲状腺c细胞肿瘤显著增加的发现与其他研究进行比较。 这项研究将被纳入因果关系整体评估中。
表2:Stout and Ruecker (1990)[78]24个月喂养研究中雄性与雌性SD大鼠中令人关注的肿瘤。
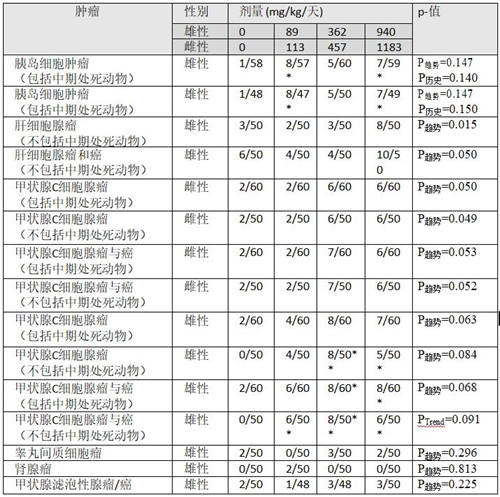
Atinson et al. (1993)[68] 对草甘膦(98.9%纯度)进行了一项慢性毒性/致癌性结合在一起的研究。他们在两种性别各自使用了50只SD大鼠,表3中列出其饮食接触剂量。还包括额外35只大鼠/性别/剂量做中间期处死。
该项研究中没有存活差异,也未表明使用的最高剂量超过最高容忍剂量。
表3:Atkinson et al. (1993)[68]SD大鼠24个月喂养研究中引人关注的肿瘤
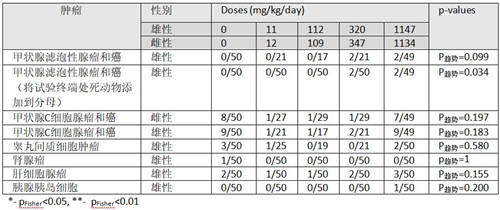
研究作者报告没有显著影响,EPA(美国环保署)[61]与EFSA(欧洲食品安全机构)[89]也如此报告。该研究没有所有组所有动物对每种肿瘤类型进行详细组织病理学检查,但是检查了所有对照组和高剂量动物,而且坚持了研究终止前死亡的所有动物和在研究终止时显示肉眼可见肿瘤的动物;还检查了所有动物的肝、肾和肺。 这严重削弱了该项研究对剂量反应趋势的研究。 然而,在回顾Greim et al.(2015)提供的病理学表格时[91],通过趋势检测发现甲状腺滤泡性腺瘤和癌有轻微显著性(p趋势= 0.099)。 如果三个中间暴露组没有看到其他肿瘤,并且分母是整个50只动物研究,趋势分析变得显着(p趋势= 0.034)。
对研究结束处死的没有大肿瘤动物进行病理检查情况下,这项研究的发现对因果关系整体评价只能给予较小权重。
Brammer (2001)[69]在Wistar鼠中进行了两年致癌性研究,每组52只动物接触草甘膦(97.6%纯度),表4列出各组剂量。额外12只动物在一年时处死。
EPA(美国环保署)指出生存率中显著阳性趋势(p=0.03),然而这样的趋势不是使用Kaplan-Meir测试[97](本应当使用的合适试验)实现的,而是简单相对与研究结束时处死动物的百分百。没有表明使用的最高剂量超过了最高容忍剂量。
EPA(美国环保署)[61],而非EFSA[89],指出与对照组比较雄鼠最高剂量组中肝细胞腺瘤有统计显著趋势。趋势分析给出p趋势=0.008,与此相比,Fisher的研究中高剂量组相对于对照组的相同测试结果为p趋势=0.027。美国环保署驳回了这一发现,可能是由于本研究与对照组的终末处死动物数量略有不同。然而,没有提供正式的生存统计评估,也不能从这些数据中推测这些动物中生存率显著受到影响。Greim et al.(2015)[91]对这种肿瘤使用了略微不同的数字,因为中期处死组中的三只动物(对照组中一个,低剂量组中一个和中剂量组中一个)在其中间处死时间之前就死亡了,从他们论文中提供的病理学表格中可以看出,它们不能与其他病例分开。这些数字被列入表4,而且并未改变研究结果的显著性。 Greim et al.(2015)[91]的研究排除了这些发现,部分原因与EPA(美国环保署)使用的生存论点相同,部分原因是他们有一个历史对照数据集,其历史响应范围为0-11.5%;他们没有提供这些历史对照的平均反应或个体肿瘤反应数据。如前所述,因为某些数据处于历史对照范围内而忽略结果是一种使用历史对照来评估研究的不可接受的方法,在这项研究情况下,没有理由对所使用的对照提出质疑。
表4:Brammer(2001)Wistar鼠24个月喂养研究中雄鼠与雌鼠令人关注的肿瘤

我获得了Charles River实验室2003年至2011年16组Wistar鼠历史性对照[98]。虽然它们超出了Brammer(2001)研究中所用动物的最佳时间范围,但它们可以说明为什么使用范围可能会产生误导。在1217只对照动物中观察到52个肝腺瘤,平均反应为4.27%,范围为0%至17.5%(个体研究结果为6/100,0/60、1/60、1/50、1/80、14/112、1/65、0/60、21/120、0/50、1/50、2/60、0/50、1/100、1/150、2/50;13个研究%响应≤2的)。假设对照组患肿瘤的潜在可能性为4.27%,p历史 = 0.006(表4)。 因此,尽管Brammer(2001)中看到的反应在历史控制范围内,但当适当使用历史控制时,这种趋势非常显著。Greim et al.(2015)也提到了在高剂量时毒性增加的发现,但他们仅提供了对于肝细胞脂肪空泡化和肝炎的数据;对任何测试这些发现均无统计学意义。
总之,这项研究显示了雄性Wistar大鼠肝细胞腺瘤的阳性结果,这项研究将纳入对因果关系的总体评估。
Suresh, (1996)[79]让Wistar鼠接触喂养中草甘膦(96.8%纯度)两年。表5中列出50只动物/性别在四组中试验的情况。
这项研究中没有生存差别,而且所使用的最高剂量没有表明超过最大容忍剂量。
EPA(美国环保署)[65]对这项研究结论没有肿瘤由于接触草甘膦增加,EFSA(欧洲食品安全机构)[89]的结论为,“任何显著显微观察的改变、发生率增加或减少(肝、脾、淋巴结、肾上腺、胸腺、性腺、子宫、乳腺中)被观察到表明剂量关系,因而看来是事故性而并非与试验成分出来相关”(第491页)。
表5: Suresh (1996)[79]的24个月喂养研究中雄性与雌性Wister鼠中引人关注的肿瘤
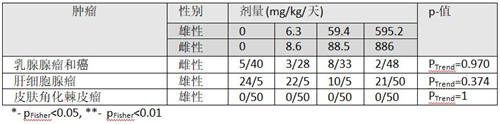
Enemoto (1997)[72]的研究中让SD大鼠接触喂养中草甘膦(95.7%纯度)两年。对四个接触组中50只动物/性别进行测试(参看表6)。此外,每个接触组10只鼠接触草甘膦1年,另外10只鼠接触18个月然后处死检查。这些组中中期处死动物(1年与18个月)如果看到肿瘤就也包括在分析中。
这项研究中没有生存差别,而且最高剂量不现实超过最高容忍剂量。
EPA(美国环保署)与EFSA(欧洲食品安全机构)在任何组中都没有发现肿瘤中显著改变。Greim et al. (2015) 再次提供了肿瘤数量表,除了雄鼠中肾腺瘤发生率(p趋势=0.004,表6)外,未显示任何其他显著效应。
对Greim et al. (2015) 提供的病理学检查表的审查,未揭示肿瘤发生率随剂量增加的任何其他肿瘤。对SD鼠进行的另外一项研究[74],显示乳腺腺瘤、甲状腺C细胞癌、皮肤角化棘皮瘤和睾丸间质细胞瘤强烈显著趋势,因此这些数据也包括在表6中进行比较。
这项研究显示肾腺瘤中显著增加,将包括在因果关系整体评估中。
表6:Enemoto (1997)[72]的24个月喂养研究中雄性与雌性SD鼠中引人关注的肿瘤
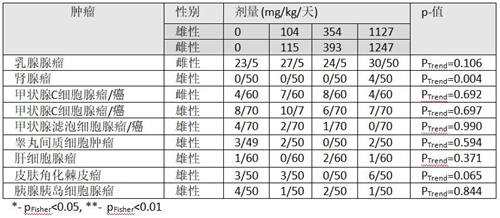
Wood et al. (2009)[80]研究中让Wistar鼠接触饲料中草甘膦(94.7%-97.6%纯度)两年。在四个接触组中对五十一只动物/性别进行试验,剂量在表7中列出。
EFSA(欧洲食品安全机构)[89]未发现随剂量增加的肿瘤,但是EPA(美国环保署)指出乳腺腺瘤和腺癌结合在一起增加而且对腺瘤p趋势=0.062,对腺癌p趋势=0.042,而对肿瘤结合在一起p趋势=0.007(表7)。EPA结论,没有腺瘤到腺癌的进展并争辩说观察到的增加非草甘膦相关。这样的结论与对照组和低剂量组中6只动物发生腺癌但是这两组中没有任何动物发生腺瘤的事实矛盾。这看来,在这种情况下,乳腺腺癌可以在不存在任何腺瘤情况下发生。
Greim et al (2015)[91]也指出雄鼠中皮肤角化棘皮瘤增加(p趋势=0.030)。对病理学表的审查没有发现任何肿瘤随剂量增加。另外一项研究发现Wistar鼠[69]中肝细胞腺瘤中强烈显著趋势,所以这种肿瘤也包括在表7中比较。
这些研究显示雌鼠中乳腺肿瘤与雄鼠中皮肤角化棘皮瘤增加,将在因果关系评价中使用。
表7:Wood et al. (2009)[80]的研究中Wistar鼠24个月喂养研究雄鼠与雌鼠中引人关注的肿瘤
联合分析
表8总结对老鼠研究中引入关注所有肿瘤的显著性。Brammer(2001)[69]观察到随着剂量增加,雄性Wistar大鼠的肝细胞腺瘤显着增加(p趋势= 0.008,表4)。 Wistar大鼠中另外两项可接受的研究(Wood等人(2009)[80]和Suresh(1996)[79])没有显著增加(表5和表7)。根据统计学显著性,这些研究相互之间不一致。
如同在硬币三次翻转中结果是一个正面和两个反面来拒绝不公平那样,仅凭1/3阳性就拒绝研究的发现也不公平,而且有更好的方式来解决这些发现。鉴于不同的剂量和不同的样本量,我们需要正式测试这些研究的一致性。
Suresh(1996)在对照组中观察到48%的肝细胞腺瘤反应,而另外两项研究在对照动物中没有看到肿瘤。因此,虽然所有三项研究都是Wistar大鼠中研究,但Suresh(1996)与另外两项研究的对照反应显著不同。 Suresh(1996)没给出使用了Wistar大鼠何种亚种,但Brammer(2001)和Wood等人(2009年)使用了Wistar大鼠不同的亚种。三项研究使用不同的饮食,并在不同的设施进行。因此,对Suresh(1996)的显著不同比率没有明显的解释。已知来自不同实验室的同品种大鼠可能具有显著不同的对照肿瘤响应。由于他们有类似的对照响应,可以将Brammer(2001)和Wood等人(2009年)的研究汇集到一项研究提出这样的问题:“将Brammer(2001)的研究与Wood等人(2009)的负面研究汇合在一起进行研究时,Brammer(2001)的显著趋势是否会消失?”对合并研究的分析得出p趋势 = 0.013,这支持了草甘膦导致具有类似背景响应的Wistar大鼠肝细胞腺瘤的结论。
Wood et al. (2009)[80] 的研究见到其他两项研究(表4与表5)中没有看见的雌鼠中乳腺腺瘤和腺癌显著增加(p趋势=0.007,表7)。这些研究中的背景发生率仅稍微不同,而且对所有三项研究在一起的汇总分析得到p趋势A=0.459,提议将这些数据结合在一起排除了Wood et al. (2009)研究中看到的剂量-响应趋势。然而,如果Suresh (1996)研究中食用的Wistar鼠对肝细胞腺瘤的响应有所不同,它们对这种肿瘤的响应可能也有所不同。仅将Wood et al. (2009) 研究与 Brammer (2001)研究结合在一起的结果为 p趋势=0.037。考虑到汇总对这种肿瘤在一起的结果,我得出的结论是它们对草甘膦可能导致Wistar大鼠乳腺腺瘤和腺癌的观点支持有限。
Wood et al. (2009)[80]的研究看到另外两项研究(表4与表6)中没有见到的皮肤角化棘皮瘤显著增加(p趋势=0.030,表7)。这些研究中的背景发生率仅稍微不同,而且对所有三项研究在一起的汇总分析得到p趋势A=0.010,提议将这些研究数据汇总在一起不排除Wood et al. (2009)的研究中见到的剂量-响应趋势。仅将Wood et al. (2009)研究与 Brammer (2001)研究结合在一起的结果为 p趋势=0.053。考虑到汇总对这种肿瘤在一起的结果,我得出的结论是它们支持草甘膦可能导致Wistar大鼠皮肤角化棘皮瘤的观点。
在SD大鼠中,有四项研究被纳入评估因果关系,其中一项[74]对雌鼠甲状腺C细胞癌与对雄鼠睾丸间质肿瘤和肝细胞腺瘤获得强烈阳性响应,其他一项[72]对雄鼠肾腺瘤产生强烈的结果。Lankas (1981)[74]的研究看到暴露于草甘膦雌鼠中甲状腺C细胞癌显著增加(p趋势=0.003,表1)以及C细胞腺瘤和癌综合分析时略微增加(p趋势=0.072, p历史=0.072,表1);其余三项研究中的一个也见到雌鼠中甲状腺C细胞腺瘤和癌略微增加(表2)。使用所有四项研究数据综合分析得到p趋势A=0.390。这样的综合分析不支持Lankas (1981)研究中看到的结果。然而,Lankas (1981)的研究为26个月,而其他三项研究为24个月;C细胞癌可能是更长暴露时间的结果,尽管研究中的剂量显著低于其他两项研究的剂量。从这些数据,我结论,草甘膦在雌性SD鼠中造成甲状腺C细胞肿瘤的证据较弱。
甲状腺C细胞腺瘤和癌结合在一起,在Stout and Ruecker(1990,表2)的研究显示边际显著剂量-响应趋势,但是其余三项研究没见到这样的趋势。将四项研究一起综合分析得到显著趋势p趋势A=0.041。从这些数据,我结论有证据表明草甘膦在雄性SD鼠中造成甲状腺C细胞肿瘤。
甲状腺滤泡细胞腺瘤和癌结合在一起,在Atkinson et al. (1993,表3)的研究显示显著剂量-响应趋势,但是其余三项研究未见这样的趋势。将四项研究一起综合分析得到显著趋势p趋势A=0.618。从这些数据,我结论没有证据表明草甘膦在雄性SD鼠中造成甲状腺滤泡细胞腺瘤。
在Stout and Ruecker (1990)的研究在雄鼠中显示肝细胞腺瘤有显著剂量-响应趋势(表2),但是其余三项研究未显示。将所有四项研究综合分析得到边际显著趋势p趋势=0.073。从这些数据,我结论有限证据表明草甘膦在雄性SD鼠中造成甲状腺滤泡细胞腺瘤。
表8:老鼠中7项研究对5种肿瘤显著测试总结
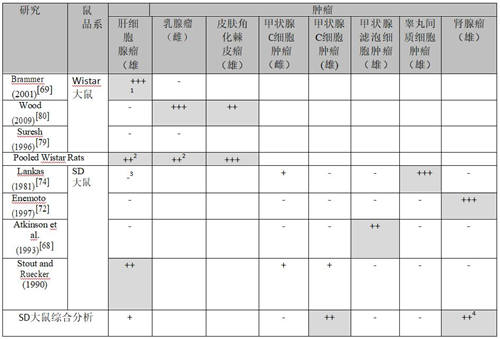
1输入值为带值的p趋势/p历史: – p>0.1, + 0.1≥p>0.05, ++ 0.05≥p>0.01, +++ p≤0.01;2仅Brammer (2001) 研究与 Wood (2009) 研究的综合分析结果;3肝肿瘤结节;4不包括Lankas (1981)研究。
SD大鼠中见到的另外一个显著趋势是Lankas(1981)[74]研究中发现的睾丸间质细胞瘤(P趋势=0.009,表1);其余三项研究对这种肿瘤阴性(表2、表3与表6)。将其余三项研究与Lankas(1981)研究结合在一起对睾丸间质细胞瘤的趋势综合分析得到的p值为清楚不显著(p趋势A=0.608)。然而,如上边注明的那样,Lankas(1981)研究是26个月研究而另外两项研究为24个月研究;这样的肿瘤可能是更长暴露期间的结果,尽管Lankas(1981)研究中使用的剂量显著低于StoutandRuecker(1990)、Atkinsonetal.(1993)与Enemoto(1997)研究中使用的剂量。
从Enemoto(1997)[72]的研究,SD大鼠中表明一种强烈显著趋势的最终肿瘤为雄鼠肾腺瘤(P趋势=0.004,表6)。Lankas(1981)[74](表1)、Atkinsonetal.(1993)[99](表3)与StoutandRuecker(1990)[78](表2)的研究中肾肿瘤数据不显著。将Enemoto(1997)的研究与Lankas(1981)[74]、StoutandRuecker(1990)和Atkinsonetal.(1993)的研究数据综合分析得到p趋势A=0.201。去除26个月的Lankas(1981)[74]研究后,其余三项24个月的研究的p值为p趋势=0.031;因此,草甘膦与肾腺瘤关联得到这些数据的支持,甚至Atkinsonetal.(1993)的研究低剂量与中剂量组结果难于解释的关联也支持这样的关联。
有证据支持暴露草甘膦增加雄性SD鼠中肾肿瘤。
总之,有证据表明草甘膦在雄性Wistar大鼠中造成肝细胞腺瘤和皮肤角化棘皮瘤,在雌性Wastar大鼠中造成乳腺腺瘤和腺癌,以及在雄性SD大鼠中造成肾腺瘤和甲状腺C细胞腺瘤和癌。有有限证据表明草甘膦在雄性SD鼠中造成肝细胞腺瘤。
小鼠研究
Knezevich and Hogan, (1983)[83]的研究中让CD-1小鼠暴露于饲料中草甘膦(99.8%纯度)两年。50只动物/组/性别在四个暴露组中测试(参看表9)。
这项研究中没有生存差异,也未表明使用的最高剂量超过最大容忍剂量(MTD)。
基于该项研究原本进行的病理学检查,美国环保署(EPA)发现肾小管细胞腺瘤在雄性小鼠中显著增加,表9显示这项分析(p趋势=0.019)。肾小管细胞腺瘤是CD-1小鼠中非常罕见的肿瘤,因此将这样的结果与历史性对照比较很重要。从事Knezevich and Hogan, (1983) 研究的实验室没有这样的历史性对照数据,因此国际癌症研究机构(IARC)、美国环保署(EPA)与EFSA(欧洲食品安全机构)全部使用了公开发表文献[101-103]中的历史性对照数据库。
对于CD-1小鼠中见到的重要肿瘤,这些研究具有几乎相同的发生率;我们将使用Giknis and Clifford (2000)[102] 的研究,因为它最好覆盖我们对于CD-1小鼠有的范围。对于进行了大约两年的研究,对照中名义历史性肿瘤响应为0.27%。将这样的对照响应率应用于肾腺瘤得到p历史=0.005,强化了该项评价对于现行对照的重要性。
美国环保署(EPA)原先使用了类似的分析并得到相同的结论。然而,在1985年,注册方聘请一组病理学家对肾切片重新检查。使用了该项研究中额外的肾切片,这些病理学家在对照动物中发现了一个额外的腺瘤,将三个腺瘤的分类改为癌(表9)。
在这些改变情况下,腺瘤不再有明显的趋势(P趋势=0.442, P历史=0.121),但是但与对现行照组相比,癌症有一定程度的显著性趋势,而且使用历史对照有明显趋势(p趋势= 0.063,p历史=0.002,历史性对照率为0.15%)。
这样的历史性对照率可能不适用于这样的分析,因为对肾腺瘤的重新评价考虑为额外的切片而没有提供这样的额外切片如何影响这样品系小鼠历史性对照发生率的信息;其他条件下可以看到差异[104]。将癌和腺瘤的发病率结合在一起与对照和历史性对照比较的显著性具有相同边际意义(p趋势=0.065,p历史=0.011,历史性对照率0.44%)。然而,对于对照组中的一个腺瘤是否被正确诊断存在相当大分歧[105]。将对照组这一个腺瘤去除的结果为p趋势=0.019与p历史=0.005。
其他的CD-1小鼠研究也见到过恶性淋巴瘤、血管肉瘤和肺腺癌(雄鼠)与血管瘤(雌鼠)。对这些研究评价那些肿瘤得到的结果不显著;对恶性淋巴瘤,p趋势=0.754, p历史=0.767,历史对照率等于6.2%;对血管肉瘤,p趋势=0.503,p历史=0.591,历史对照率等于2.5%;对肺腺癌p趋势=0.918,p历史=0.899,历史对照率等于9.2%,对血管瘤p趋势=0.631。该研究中没有发现其他的肿瘤。
美国环保署(EPA)[61]提出了许多不同观点来驳斥本研究中肾肿瘤的发现。
观点之一是美国环保署(EPA)要求的病理学工作组1986年结论这些病变与草甘膦无关因为“1)肾小管细胞肿瘤是自发性病变,对这种小鼠只存在少量历史对照数据; 2)处理组与现行对照组配对比较没统计学显著性,并且没有统计显著线性趋势证据; 3)任何动物中未发现多个肾肿瘤; 和4)在这项研究中,雄性小鼠中不存在肿瘤前变化等化合物相关肾毒性损伤。”
理由一不再存在,因为有对于CD-1小鼠两个非常好的历史对照数据库[101, 102]。
理由二,尽管技术上正确,也不具有支持性,因为环保署自己评价致癌性研究的指导原则指出:“任何一种测试[趋势或成对]的重要性都足以驳斥结果偶然的假设。”
理由三也软弱,因为处理罕见肿瘤时不会期望出现(也不需要期望)多种肿瘤。
对于理由四,环保署(EPA)提供了研究中双侧慢性间质性肾炎发生率的数据,他们认为显示没有统计显著性结果,尽管趋势测试高度显著(p趋势=0.006,表9 )。EP在没提及参考文献依据情况下指出,“慢性间质性肾炎不被认为是肾小管肿瘤的前兆病变”。
我找不到支持或者反驳这种说法的公开发表文献。然而,慢性间质性肾炎是肾脏中肾小球和小管周围间质组织炎症。众所周知,炎症在肾癌[106]和许多其他癌症中发挥重要作用,因此这一论点也未能支持对这些发现的拒绝。
表9、Knezevich and Hogan, (1983)[83]24个月喂养研究雄性与雌性CD-1小鼠中令人关注肿瘤
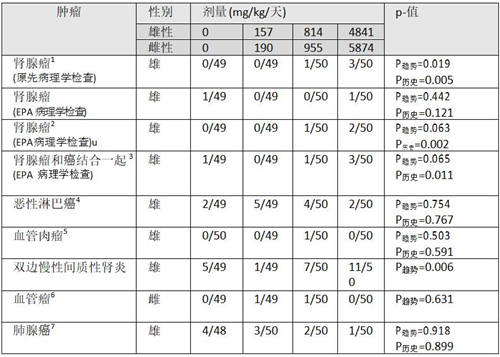
总之,这项研究显示在雄性CD-小鼠中肾肿瘤阳性结果,将被包括在因果关系总体评价中。
Atkinson, et al., (1993)[81] 的研究中将CD-1小鼠暴露于饲料中草甘膦(纯度>97%)两年。五十只动物/组/性别在四个处理组中测试(参看表10)
没有看到服用草甘膦对生存的影响,也没有表明高剂量超过最高容忍剂量(MTD)。
表10:Atkinson, et al., (1993)[81]24个月喂养研究雄性与雌性CD-1小鼠令人关注的肿瘤
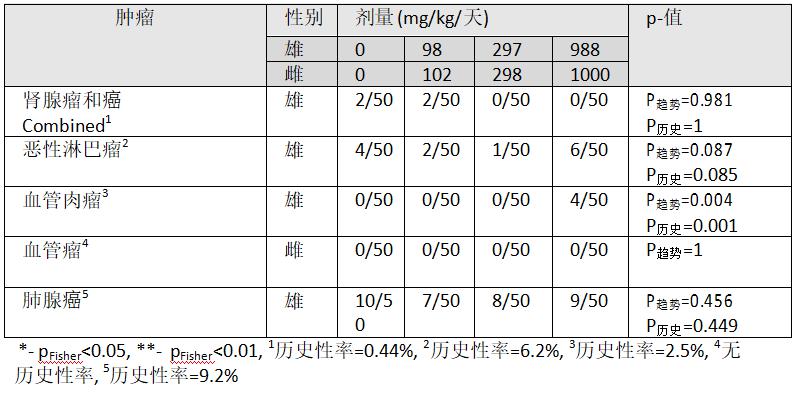
血管肉瘤是这项研究中显示显著趋势的唯一肿瘤(P趋势=0.004, P历史=0.001,表10 )。表10中也显示恶性淋巴瘤、肾肿瘤与肺腺癌(雄鼠)与血管瘤(雌鼠)的结果;恶性淋巴瘤有边际趋势(P趋势=0.087, P历史=0.085),肾肿瘤没有趋势。
环保署(EPA)结论这项研究中的发现与处理无关,他们的理由是这些肿瘤仅出现在高剂量组,缺乏这一组中的响应与对照组响应之间统计显著性,以及这些肿瘤在小鼠中通常可以观察到,既自然发生也作为相关影响。
没有排除最高剂量组中阳性发现的科学文献支持,这也是SAP的看法[54]。我已经评论过EPA如何处理趋势测试和Fisher's Exact测试结果的指导方针,尽管在这种情况下,最高暴露组与对照组之间的比较值pFisher = 0.059略微显著。
【译注:FIFRA(Federal Insecticide, Fungicide, and Rodenticide Act)--联邦杀虫剂、杀真菌剂与杀鼠剂法;SAP(Science Advisory Panel)--环保署FIFRA的科学咨询专家组。】
对于对照中肿瘤发生频率的争论直接通过评估历史对照率来解决; 如果这些比率足以排除这一发现,P历史将会高于0.05而不是0.001。
CD-1小鼠的两年癌症生物测定对照中血管肉瘤的平均历史对照发生率为2.5%,高剂量组中见到的响应为8.9%。
SAP清楚指出,环保署(EPA)使用的由于历史对照数据否定肯定了的发现的操作,是不可接受的[54]。第63页)环保署(EPA)的癌症知道原则对此清楚指出“统计显著的肿瘤增加不应该仅仅因为处理组发生率在历史对照范围内或因为现行对照发生率略低于平均水平而忽略。”
总之,这项研究显示雄性CD-1小鼠中血管肉瘤肯定结果,将被包括在因果关系总体评价中。
Wood et al., (2009)的研究[88]将CD-1小鼠暴露于饲料中草甘膦(纯度95.7%)80周。51只动物/组/性别在四个暴露组中测试(参考表11)。
没有对生存的影响,也没有信息提议该项研究超过最高容忍剂量(MTD)。
这项研究中未见肾肿瘤或血管瘤(雄鼠)或血管瘤(雌鼠)增加。雄鼠中有肺腺癌单调增加(p趋势=0.028, p历史=0.031)与恶性淋巴瘤单调增加(p趋势=0.007, p历史=0.007)。这项研究的历史性对照发生率与早期的研究不同,因为这项研究仅为80周而非早期研究那样104周(两年);80周后CD-1小鼠中对恶性淋巴瘤的历史性对照发生率为2.6%而不是两年研究历史性对照发生率的6.2%[102]。
对于肺腺癌,环保署(EPA)[61] 再次认为配对比较缺乏重要性(违反自己的指南),并且没有证据表明从腺瘤发展到癌症。尽管肺腺瘤的增加不显示为暴露的函数,但是肺腺癌可能在没有相关腺瘤增加情况下增加[107]。
对于恶性淋巴瘤,环保署(EPA)指出有统计显著响应而且高剂量组与对照相比显著不同(pFisher=0.028),但是随后基于本研究进行的分析次数将Fisher Exact测试p值调整为0.082(评估这些动物癌症研究结果时,确实需要对多重比较进行调整,我的报告后边评价所有综合研究时将讨论这个问题)。
美国环保署(EPA)[61]使用历史性对照数据[103, 108]排除恶性淋巴瘤并引用平均回应率为4.5%,范围为1.5%至21.7%。Son and Gopinath (2004) 的研究[108]在1453只动物中在80周以前看到21只动物有肺腺癌(1.4%)。
GiknisandClifford(2005)[103]的研究在大部分为78周对照(26项研究)与104周对照(21项研究)的52项研究中看到平均发生率为4.5%,范围为0%与21.7%。仅包括80周或更短期间研究情况下,GiknisandClifford(2005)[103]研究为37/1372=2.7%,范围0%至14%。GiknisandClifford(2000)[102]研究(我曾引用其参考文献)进行了类似评价,使用与他们2005年研究大部分相同的数据见到80周前平均肿瘤发生率2.6%,范围0%至14%。基于环保署(EPA)对GiknisandClifford(2005)研究历史性对照进行的有缺陷的解释,EPA认为研究现行对照的发生率很低(为0%),并拒绝了该研究的阳性结果。
事实上,在Giknis and Clifford (2005) 研究中评价的18个月对照组中的26项研究,八项(31%)的响应为0%而另外八项(31%)仅有一个肿瘤。美国环保署(EPA)使用的评价不正确。此外,如前边指出的那样,美国环保署(EPA)的指导原则[33, 54] 或其科学咨询专家组(SAP)[54]不同意用历史性对照数据否定肯定性发现。
有多重恶性肿瘤动物的数量有所增加(P趋势=0.046)。
总之,该项研究显示雄性CD-1小鼠重恶性淋巴瘤与肺腺癌肯定性结果,将包括在因果关系总体评价中。
表11:Wood et al. (2009)[88]18个月喂养研究雄性与雌性CD-1小鼠中令人关注的肿瘤
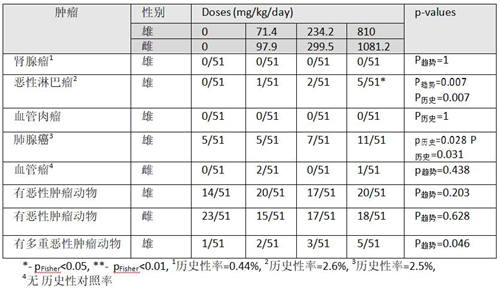
Sugimoto (1997)的研究[87]中CD-1小鼠暴露于饲料中草甘膦(纯度94.61-95.67%)两年。
处理对生存没有影响而且没有表明最高剂量超过最高容忍剂量。
雄小鼠中肾腺瘤(p趋势=0.062, p历史=0.005)、恶性淋巴瘤(p趋势=0.016, p历史=0.017)与血管肉瘤(p趋势=0.062, p历史=0.004)与雌小鼠中血管瘤(p趋势=0.002)显示肿瘤发生率随剂量增加而增加。雄小鼠中肺腺癌的评价显示没有显著剂量--相关趋势(p趋势=0.148, p历史=0.140)。这项研究中也显示雄性动物中任何恶性肿瘤都增加(p趋势=0.001),但雌性动物中没有。
应注意到Giknis and Clifford (2000) 研究的26个对照组中没有看到血管肉瘤,因此对历史对照响应估计发展是困难的(如果历史对照率为0,则除0之外的任何观察响应具有0的p值)。历史对照中从来没有见到这种肿瘤的事实,应强烈支持任何肯定性发现具有显著性。然而,为了依然允许食用历史性对照数据的测试,我使用了平均反应的历史对照估计值,结果在1149只动物中有5%机会看不到肿瘤。这样预计的历史性对照响应值为0.0026。对暴露18个月CD-1小鼠中血管肉瘤的分析中使用了该值(p历史 <0.001)。
表12:Sugimoto (1997)的研究[87]中雄性与雌性CD-1鼠中令人关注的肿瘤
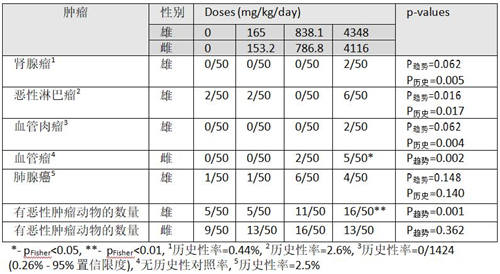
美国环保署(EPA)[61] 仅讨论了雌性小鼠血管瘤,并没有注意到任何其他显著影响。 对于雌性小鼠来说,EPA认为高剂量大约是目前经合组织指南推荐的高剂量的四倍[109]。 这项研究根据以前的指南正确设计(限值<5%,饲料中),没有迹象表明该剂量超过了最高容忍剂量(MTD)。 美国环保局还指出,当Fisher's Exact检验测试的p值被调整为多重比较时,高剂量血管瘤组的新p值为0.055。
对于雄性小鼠中血管肉瘤,Giknis and Clifford (2000) 的研究中审查的26项历史性对照组中没有一个有血管肉瘤,使其成为雄性小鼠80周前发生的非常罕见肿瘤。雄性小鼠中的恶性淋巴瘤相对于现行对照组以及历史性对照都统计显著。最后,雄鼠中恶性肿瘤总体上清楚增加。
总之,这项研究对雄性CD-1小鼠中肾腺瘤、恶性肿瘤与血管肉瘤显示肯定性结果,对雌小鼠中血管瘤显示肯定性结果,而且在雄性CD-小鼠中显示恶性肿瘤随暴露总体增加。这项研究将包括在对因果关系总体评价中。
Kumar (2001) 的研究[84]中将瑞士小白鼠暴露于饲料中草甘膦(>95%纯度)两年。五十只动物/组/性别在四个暴露组中测试(参看表13)。
生存率在最高暴露组中减少,但并不统计显著,而且没有其他数据显示该项研究超过了最高容忍剂量(MTD)。
雄小鼠中肾腺瘤(p趋势=0.062)与恶性淋巴瘤(p趋势=0.064, p历史 =0.070)显示边际统计显著,但是雄小鼠中血管肉瘤(p趋势=0.500)显示不统计显著。这项研究中,并没有对低剂量与中剂量组所有动物进行肾肿瘤评价,因此对这两组经过检查的动物进行了第二次分析(p趋势=0.088)。对于瑞士Albino小白鼠中血管肉瘤与肾腺瘤没有历史性对照数据。
对于恶性淋巴瘤,欧洲食品安全机构(EFSA)提供了一组历史性对照数据显示平均响应46/250=0.184(18.4%)范围为6%至30%。使用这组历史性对照数据,趋势仅边际显著(p历史=0.070)。
我对两个剂量在历史性对照范围之外而第三个剂量在历史性对照范围的上限有某些担心。然而,这个历史性对照数据组对于相对高背景肿瘤率而言很小,因此过于强调这样一个历史性控制群体是不合理的。
最近的一个备忘录中,Martens (2017)[110]断言Greim et al. (2015)的研究[91] 与 EFSA (2013)[89] 中出现的恶性淋巴瘤与肾腺瘤的发生率计数不正确并提供了不同发生率(见表13)。使用来自Martens备忘录的发生率计数,对于这两种肿瘤的p-值皆降低了。
然而,应当指出,如果Martens (2017) 备忘录中对于恶性淋巴瘤的计数正确的话,那么所有三个暴露组的响应都在历史性对照凡物之外。从Greim et al. (2015)、 EFSA 或 Martens (2017)备忘录来看,不清楚哪种肿瘤发生率计数正确。
雌小鼠中血管瘤(任何组织)中有显著增加(p趋势=0.004)。
总之,对于雄性瑞士Albino小白鼠中恶性淋巴瘤与肾腺瘤随暴露而增加,以及雌性小白鼠中血管瘤增加,这项研究给予支持。这项研究将包括在对于因果关系总体评价中。
表13:Kumar (2001)[84]对雄性与雌性瑞士Albino小白鼠18个月喂养研究中令人关注的肿瘤

George et al. (2010) 的研究[82]将20只瑞士Albino小白鼠暴露于25mg/kg(草甘膦等同剂量)草甘膦配方制剂(农达,36g/L草甘膦),局部每周一次接后一周三次12-O-十四烷酰佛波醋酸酯-13(TPA),每周三次,局部每周三次持续三周,接后一周TPA每周三次,或者一次局部应用7,12-二甲基苯并[a]蒽(DMBA)接后一周局部应用草甘膦每周三次总共期限为32周。也包括适当未处理、DMBA处理与TPA处理对照。暴露于DMBA接后草甘膦的组显示有肿瘤动物数量显著增加(p<0.05)(处理动物40%有肿瘤、对照动物无肿瘤),表明草甘膦对皮肤两阶段模型中致癌作用具有促进作用。本研究解决了草甘膦是否更容易通过启动(开始癌症过程)或促进(在开始后推动过程)引起皮肤肿瘤的问题。 这项研究支持草甘膦可以对肿瘤发病率产生影响的整体概念。
美国环保署(EPA)[61]对降低该研究的意义,声称它仅包括每组20只动物,仅测试了雄性,未进行组织病理学分析。 很难理解EPA如何拒绝使用20只小鼠的阳性结果; 通常情况下,人们会忽略研究动物数量太少的一项负面研究,因为没有足够的统计力来查看效果,但从来不会因为这个原因拒绝正面结果。 另外,每组20个动物对于皮肤描述的启动促进研究是常见的,如在此提出的研究。 仅在雄性中进行研究并不是忽视研究中肯定性发现的理由。 最后,在小鼠皮肤的启动 - 促进研究中,如果有兴趣从癌中分离乳头状瘤,将进行组织病理学评估。DMBA /草甘膦处理的小鼠中 40%看到的损伤不是乳头状瘤或癌不大可能。
美国环保署(EPA)科学咨询组(SAP)某些成员指出[54],啮齿动物的数据与作为肿瘤启动子的草甘膦是一致的,但是,因为“这里并没有直接检验这个假设(如在标准启动促进生物测定中)......”这个结论是推测性的。(第#页)。 由于美国环保署(EPA)没有进行任何讨论就驳回了这项研究,因此科学咨询组(SAP)没有认识到草甘膦有启动--促进作用,这支持了草甘膦有促进这样过程的效果。
该项研究被包括在因果关系评价中,因为该项研究支持草甘膦对某些肿瘤的促进性作用。
联合分析--小鼠
在他们对小鼠研究的评估中,美国环保署(EPA)[61]和欧洲食品安全机构(EFSA)[89]选择分别挑战每项研究的结果,驳斥研究说它们没有效果,并且从未比较各种研究的结果。 根据国际癌症研究机构(IARC)[30]的评估,EFSA [90]提取了原始数据,并对5项小鼠研究中的雄性小鼠的肾肿瘤、恶性淋巴瘤和血管肉瘤进行了趋势测试,这也是我认为可以接受 进行因果分析的五项研究。美国环保署(EPA)和欧洲食品安全机构(EFSA)只是制作了一张表格,列出每个研究中每个剂量组的响应,并且(主观地)认为它们不一致,而不是通过综合适合的数据正式评估这些癌症反应的一致性。 此外,美国环保署(EPA)和欧洲食品安全机构(EFSA)认为,超过1000毫克/千克/天的剂量(其中只有两种如此)超出了经合组织(OECD)指导方针现行测试范围,认为应予排除。 我在下边将讨论这两点。
在CD-1小鼠中,有四种有用的动物致癌性研究和一项瑞士Albino小白鼠研究。 与大鼠一样,可以通过两种方式解决探讨它们之间的一致性。首先是通过简单查看总体结果来评估他们在统计显著性方面的一致或不一致。表14总结了所有五种癌症的阳性和阴性结果,其中CD-1小鼠中至少一项研究显示出显著趋势。很显然,并非每种肿瘤在每项研究中都显示草甘膦暴露呈阳性趋势。 对于雄性血管肉瘤, Sugimoto (1997) 和Atkinson et al. (1993) 的研究显示明显的肯定性结果。Wood et al. (2009) 与Knezevich and Hogan (1983)则没有显著性响应。雌性血管肉瘤仅出现在Sugimoto (1997)的研究中。
雄性中恶性淋巴瘤在两项研究中显然为阳性[87,88],而在第三项[81]中略微阳性,但在第四项中为阴性[83]。 这两项强阳性研究都将动物暴露了18个月。雄性肾脏肿瘤在两项研究中为阳性[83,87],而在其余两项中为阴性[81,88]。在Wood et al. (2009)的研究中,只有在雄性中肺腺癌有阳性。Sugimoto (1997) 在肿瘤和草甘膦之间有四项明显阳性关联,而其他的只有两项或更少这样的关联。
表14:CD-1小鼠中4项研究5种肿瘤显著测试总结
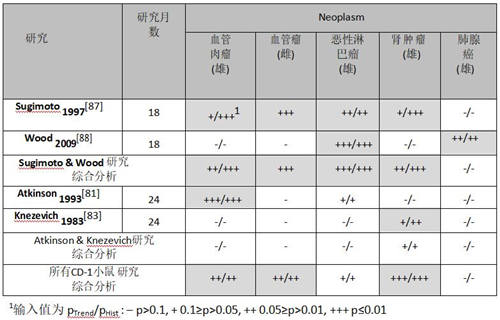
如同在大鼠研究中看到的那样,对阳性与阴性结果的这种简单评估未能解决这些数据的整体反应中哪些发现正在推动的问题。要做到这一点,我将再次汇集研究成果。表14总结了汇总分析。
对于雄性肾脏肿瘤,汇集两项18个月的研究显示发病率显著增加(p趋势 = 0.015,p历史 = 0.003),两年研究的汇总显示边际显着性(p趋势 = 0.081,p历史 = 0.054)。汇集所有四项研究的结果(p趋势= 0.005,p历史 = 0.007),因此仍有肯定性趋势。 Knezevich and Hogan (1983)的研究在其最高接触组中观察到4%的肾癌响应。 Giknis and Clifford (2000)中的48项研究以及Giknis and Clifford (2005)中的52项研究中对照组肾癌的最大反应为2%,11项为期两年的癌症研究对照组, Chandra and Frith (1992)[101]研究中在725例中仅见到一例肾癌。
在46组对照数据组中,Giknis and Clifford (2000) 的研究看到39组对照组没有腺瘤,5组有一个腺瘤与两组中有两个腺瘤;两项24个月研究在最高暴露组中见到两个腺瘤,这是非常罕见的发现。
为更好说明,四项研究中共有16组动物。对于任何一个组来说,获得4%或更大响应的几率为2/44或4.3%。
在16个组中随机获得3个或更多这样响应的几率为2.9%,并且其中两个为四个最高接触组中任何两个的几率为0.01。总之,四项研究中的两项研究的强烈发现与四项研究汇总均为阳性结果,以及与历史对照相比几率很低的这样的结果,支持草甘膦导致雄性小鼠肾脏肿瘤的结论。
对于雄性中的恶性淋巴瘤,汇集了两个为期18个月的研究,Sugimoto(1997)和Wood et al.(2009),导致显著的趋势(p趋势= 0.005,p历史= 0.006)。汇集两个为期24个月的研究,KnezevichandHogan(1983)以及Atkinsonet al.(1993),得到(p趋势= 0.653,p历史= 0.649)。 这两个发现的主要区别在于对照响应;24个月的汇总对照响应为6/99(6%),而18个月的则为2/101(2%)。 这是可预料的,因为在没有任何暴露的情况下,肿瘤发生率随着年龄的增长而增加[5]。Giknis and Clifford (2000)在18个月时的对照响应率为4%,24个月时的对照响应为6%(与汇总研究值相匹配)。 汇集所有四项研究结果(p趋势A= 0.073,p历史= 0.080)。
然而,Giknis和Clifford(2000)在对照组中观察到的恶性淋巴瘤的反应在26个18个月的组中仅显示一个历史对照组,并且具有10%或更高的反应。在两个为期18个月的研究中,高剂量(10%和12%)的反应几乎不可能偶然出现。这两项研究中有八组动物。对于任何一组,根据Giknis和Clifford(2000)的26个对照组,获得至少10%的回答的可能性为1/26或3.8%。在八组中得到两个或更多这样的响应的机会是0.035,并且这四个最高接触组中的三个的机会是0.004。对于24个月的研究,较高的背景发生率使得很难确定发生率的微小变化,因此24个月研究和18个月研究中的发现并不矛盾。总之,18个月的研究得出的结果非常好,两个为期18个月的研究汇总得出的强烈的阳性结果,在18个月的研究中观察到的反应的概率很低,都是偶然的,边际瑞士白化小鼠18个月的研究中恶性淋巴瘤的增加支持了草甘膦导致雄性小鼠恶性淋巴瘤的结论[84]。
对于雄性血管肉瘤,将这两项为期18个月的研究汇总在一起结果为显著趋势(p趋势= 0.015,p历史 = 0.002)。合并两个24个月研究结果(p趋势 = 0.490,p历史 = 0.429)。这两个发现的主要区别是Knezevich and Hogan (1983)研究中暴露于4841 mg / kg /天的动物0/50响应。在汇集的24个月分析中去除这一个暴露组得到(p趋向<0.001,p历史 <0.001)。汇集所有四项研究的结果(p趋向= 0.045,p历史 = 0.043)。Giknis and Clifford (2000)的二十六个18个月研究中,未观察到血管瘤,因此Sugimoto (1997)在高剂量组中观察到的两个血管肉瘤在生物学上非常重要。对于24个月的历史对照,20个对照组中仅有2个的反应超过8%。总之,18个月研究中的非常强烈的发现,所有四项研究汇总时的阳性结果以及18个月研究中观察到的反应的低概率,都是由于支持草甘膦导致雄性血管肉瘤结论CD-1小鼠的机率。
对于雌性血管瘤,将这两项为期18个月的研究汇集在一起的结果为显著趋势(p趋势 = 0.001)。汇集两年研究的结果p趋势 = 0.424。汇集所有四项研究的结果p趋势 = 0.018。总之,在一项为期18个月的研究中非常有力的发现,所有四项研究汇总后的肯定结果以及认为Sugimoto(1997)研究中发现的响应偶然的低概率,支持草甘膦导致雌CD-1小鼠中血管瘤的结论。
对于雄性CD-1小鼠中的肺腺癌,汇集两个18个月的研究结果显示没有显著趋势(p趋势 = 0.417,p历史0.126)。 汇集两个24个月的研究结果(p趋势A = 0.985,p历史 = 0.993)。 汇集所有四项研究的结果(p趋势A = 0.937,p历史 = 0.744)。 总之,一项24个月研究中的中等发现和任何研究汇集时的阴性结果表明,雄性CD-1小鼠中草甘膦与肺腺癌之间的联系是偶然的。
瑞士Albino小白鼠的一项研究[84],对恶性淋巴瘤和肾腺瘤发现有轻微肿瘤响应,对其他终点都阴性。 考虑到 Kumar (2001)研究中CD-1小鼠肾腺瘤的研究结果,草甘膦也可能导致雄性瑞士小白鼠肾腺瘤。
总结小鼠研究中的发现,草甘膦在暴露18个月后在雄性CD-1小鼠中引起血管肉瘤、肾肿瘤和恶性淋巴瘤,在雌性CD-1小鼠中引起血管瘤;暴露24个月后在雄性CD-1小鼠中引起肾肿瘤,并可能在雌性瑞士小白鼠中引起肾脏腺瘤。汇集18个月的研究和24个月的研究在一起,雄性小鼠血管肉瘤,雌性小鼠血管瘤和雄性小鼠肾肿瘤显著增加。
动物致癌性研究讨论与总结
在评估动物致癌性研究的结果时,... 在OECD指南[59]的第90段中清楚地列出了动物致癌性研究中排除某种剂量的原因[59]:
“如果该研究的主要目的是确定癌症危险,广泛接受其中的最高剂量应当是理想情况下依据所提供一些毒性迹象,例如轻微抑制体重增加(不超过10%),而不引起例如组织坏死或代谢饱和,并且由于除了肿瘤以外效应而基本上不改变正常寿命。 最高剂量水平(或任何其他剂量水平)的过度毒性可能会损害研究的有用性和/或所生成数据的质量。 为了选择足够的最高剂量水平而发展的标准包括:(特别是)毒代动力学; 吸收饱和度; 先前重复剂量毒性研究的结果; MOA(作用机制)和MTD(最高容忍剂量)。”
一项研究虽然发生体重增加略有下降,但在任何其他研究中都没有迹象表明任何剂量超标都会支持忽视任何暴露组的结果。
美国环保署(EPA)[33]根据早期经合组织(OECD)文件,采用略有不同的标准确定包含或排除哪种剂量。这些在EPA的致癌风险评估指南文件中有详细说明[33]:
“与过量高剂量相关的其他处理相关毒性征兆可包括(a)体重增加率显著减少(例如,大于10%),(b)异常行为和临床体征显著增加,(c)显著变化 (d)吸收和解毒机制的饱和,或(e)器官重量、形态学和组织病理学的显著变化。 应该注意的是,已经建立了实际的上限,以避免在环境化学品的长期致癌性研究中使用过高剂量(例如饲料中测试物质的5%用于饮食研究或1g / kg体重 用于口服灌胃研究[OECD, 1981])。”和以前一样,这仅适用于本次审查中提出的一项研究。
这两条准则都具有良好的科学意义。 在本评估收入的12项可接受的啮齿动物致癌性研究中,没有一项研究在最高剂量时具有足够的毒性来证明从分析中去除最高剂量合理。 因此,这里提出的分析没有去掉> 1000毫克/千克/天的剂量。 这也得到了EPA SAP(科学咨询专家组)的一位成员的支持[54]。
使用草甘膦作为测试化合物已经进行了20项慢性啮齿动物致癌性研究。这些研究中有8项不适用于评估因果关系,留下了七项大鼠研究和五项小鼠研究。由于在个体动物致癌性研究中进行了大量的评估,因此担心假阳性率可能会被夸大。例如,如果完成了20次评估,并且如果p趋势 <0.05,则应认为发现是显著的,那么您可能会认为20 * 0.05 = 1的评估仅仅是由于机率而为肯定性。
表15:使用草甘膦的12项接受的啮齿动物致癌性研究中观察到的与预期具有显着趋势肿瘤部位

动物致癌性研究结论
存在与所有动物致癌性研究有关的几个一般性问题。随着时间和空间的变化,跨动物品系的遗传变异也很大。即使使用相同的动物品系,也很难比较在不同实验室进行的实验。当您在使用该品系的三项研究中检查Wistar大鼠肝细胞腺瘤的发生率时,这一点很明显。因此,在对各个研究进行比较之前,应对每个研究的研究结果分别进行考虑。
使用p值0.05作为增加肿瘤发生率的临界值并不能说明多项研究的数据趋势。汇集进行分析的三项研究在给定肿瘤中边缘反应为6-8%的研究可能会导致非常重要的发现。由于缺乏重复研究,该问题在流行病学中已得到公认,但在毒理学中通常不予考虑。这种情况是相当独特的,因为有大量可用于分析的研究,并且需要对数据进行更严格的评估,例如本报告中介绍的汇总分析。
汇总数据以评估重复研究是有意义的,因为它解决了“这些数据是否整体上支持这些研究中癌症发病率增加的发现?”这一问题。一些毒理学家可能会争辩说,这些研究不是重复的,因此无法汇总。但是,如果它们不是重复项,则无法将它们进行比较以查看研究之间是否存在一致性。这是因为从一项研究到另一项研究可能会有一些细微的变化,从而导致一项研究的结果为阳性,而其他研究的结果为阴性。他们因此认为,研究不是很好的重复样本,因此您无法在各个研究之间进行比较,也无法合并它们;或者它们是很好的重复样本,因此您可以在各个研究之间进行比较,然后合并它们。当合并不合适时,没有理由支持跨研究的比较。
有七项大鼠研究和五项小鼠研究具有足够的质量,并且有足够的细节可纳入草甘膦已被证明在两只老鼠和一只老鼠中引起癌症的本评估。
草甘膦在雄性Wistar大鼠中引起肝细胞腺瘤,并在较小程度上在雄性Sprague-Dawley大鼠中引起雌性Wistar大鼠乳腺腺瘤和腺癌,在雄性Wistar大鼠中引起皮肤角膜癌,肾脏腺瘤和甲状腺C细胞腺瘤和癌。在雄性Sprague-Dawley大鼠中。草甘膦可引起雄性CD-1小鼠的血管肉瘤、肾脏肿瘤和恶性淋巴瘤,以及雌性CD-1小鼠的血管瘤,并可能引起雄性瑞士白化病小鼠的恶性淋巴瘤、肾腺瘤和雌性瑞士白化病小鼠的血管瘤。因此,草甘膦在哺乳动物中引起癌症。
与致癌性有关的机制
许多人类致癌物通过多种机制起作用,引起各种生物学变化,使细胞经历从正常运行到几乎没有或几乎没有生长控制的致癌性(致癌)的多个阶段。 Hanahan和Weinberg(2011)[112]识别了细胞在此多阶段过程中进展时的形态变化,并将其与遗传改变相关联,从而开发出了所谓的“癌症标志”。这些标志涉及整个致癌过程,并不一定涉及细胞开始该过程或该过程早期的原因,在该过程中,细胞内的正常保护系统会从体内清除潜在癌性细胞。虽然通过化学分析对细胞造成的伤害可能通过突变分析与其他肿瘤有所区别,但它们均具有Hanahan和Weinberg(2011)所描述的特征。
由于缺乏广泛接受的评估机理数据的方法来得出有关致癌相关人类危害的客观结论,因此有关化学物致癌机理的所有数据的系统综述变得复杂。这种系统的方法在其他情况下存在[113],但直到现在才被接受为毒理学评估中评估文献的一种手段[114-117]。
在报告的这一部分中,我将重点介绍可能导致癌症的机制。Smith et al.(2015)的研究[37]讨论了使用系统评价方法来识别和使用文献中的关键信息来表征化学物质致癌的机制。他们确定了10个“癌症的关键特征”,可用于促进系统性和统一的方法来评估与致癌物有关的机制数据。表16中列出这10个特征(从Smith et al. (2015)[37]的表1复制)。尽管草甘膦具有大多数关键特征的证据有限,但基因毒性(特征二)和氧化应激(特征五)有足够的证据值得全面审查。
基因毒性
基因毒性是指试剂(化学性或其他物)破坏细胞内遗传物质的能力,从而增加发生突变的风险。基因毒性物质与遗传物质DNA序列和结构等相互作用,破坏细胞。 DNA损伤可以通过几种不同的方式发生,包括单链和双链断裂、DNA碱基与蛋白质之间的交联、微核的形成以及DNA的化学添加。
仅仅因为化学物质会破坏DNA并不意味着它会引起突变。因此,尽管所有引起突变的化学物质都具有基因毒性,但是所有基因毒性化学物质不一定都是诱变剂。如果用于识别暴露于化学物质后细胞中突变的所有测定均为阴性,这是否意味着可以忽略化学物质的基因毒性?这个问题的答案是否定的,并且与诱变性测试(一种化学物质在细胞中引起突变的能力)的局限性有关。在暴露前对整个基因组的序列进行评估,然后在暴露后用相同的序列来确定基因组是否已被改变(突变),这是很不寻常的。有一些检测方法可以评估一组先前与癌症结果相关的关键基因(例如癌癌基因),但很少应用。通常,致突变性测试受限于它们实际筛选的基因数量以及这些筛选的工作方式。
由于对致突变性的筛查范围有限,因此由化学物质引起的任何遗传损害都应引起关注,因为这种遗传损害可能引起突变。在下文中,我将系统地回顾可用于评估草甘膦基因毒性潜力的科学发现。根据该数据的生物学来源,它将分为六个单独的数据源:(1)来自暴露的人类的数据,(2)来自实验室环境中暴露的人类细胞的数据,(3)来自暴露的哺乳动物(非人类),(4)来自实验室中哺乳动物(非人类)暴露细胞的数据,(5)来自非哺乳动物和其他动物的数据,以及(5)来自非哺乳动物和其他动物的细胞的数据。这六个领域的基础是影响方面的优先领域。在人类中发现基因毒性比在其他哺乳动物中发现基因毒性更重要,而哺乳动物中发现基因毒性比在非哺乳动物系统中看到基因毒性更重要。此外,与在实验室(体外)细胞中观察到的反应相比,在整个活的生物体(体内)观察到基因毒性的权重更大。基本上,研究结果离真实的活着的人类越近,就应该给予更多的重视。
表16:致癌物的主要特征,Smith et al. (2016)[37]

本次审查中的数据来自经过同行评审的科学文献,以及我专有的但无法访问其原始著作的法规文件中的报告摘要,以及来自我所从事工作中有很大访问权限的行业专有报告。 所有这些研究都包括在因果关系的总体评估中。
体内人类的基因毒性
三项研究评估了草甘膦制剂在暴露于人体中的潜在基因毒性。Paz-y-Miñoetal.(2007)[118]使用彗星分析法分析了24名暴露者个体(在喷洒场地3公里之内生活)和21名未暴露者个体(在喷洒场地80公里外生活)的血液对DNA的损伤。所有研究对象均来自厄瓜多尔,在正常的日常生活过程中,没有对照组或暴露人群吸烟、饮酒、服用非处方药或接触过农药。接触者和对照者进行了一些耕种和收获,但没有接触农药或除草剂。为清除与非法麻醉品有关的植物喷洒(草甘膦除草剂)后两个月内对暴露者个体进行了分析。根据彗星尾巴中的DNA量,在0-400之间对每人平均200个细胞进行排列,以计算平均DNA损伤量。暴露于对照组的个体的平均总迁移水平之间存在显着差异(p <0.001)。根据彗星尾巴中的DNA量,将每个人的数据分为五组。显然,DNA在细胞中的分布发生了变化,而对照组,除三名外,从未在前两类中看到得分,其他人在前两类中都有一些得分。从本质上讲,某些DNA已因暴露而断裂。
研究中,Paz-y-Miñoetal.(2011)[119]评估了厄瓜多尔北部10个社区的92个人的核型(在显微镜下观察到的个体的染色体数和染色体的任何改变)。对照来自没有喷洒(草甘膦除草剂)的区域,并且对照和暴露的受试者都没有暴露于吸烟或其他基因毒性化合物的历史。评估了182个核型中,这项研究发现对照和暴露对象之间没有发生变化。
Bolognesietal.(2009)[120]在哥伦比亚的五个地区研究了育龄妇女及其配偶,其中四个地区需要喷洒除草剂以控制毒品或种植甘蔗。有60位受试者来自Santa Marta地区(种植无需使用农药的有机咖啡),52位来自Boyaca(人工喷洒非法毒品作物),58位来自Putumayo(用飞机从空中对非法毒品作物喷洒草甘膦制剂),来自Nariño的63位受试者(与Putumayo的暴露相同)和Valle del Cauca的28位受试者(从空中喷洒农达除草剂Roundup 747,草甘膦含量占74.7%,对甘蔗作为催熟剂,无需额外的辅助剂)。所有受试者均接受了标准化问卷调查,该问卷旨在获取有关当前健康状况、健康史、生活方式以及潜在的可能混杂因素(吸烟、使用药品、最近六个月内的严重感染或病毒性疾病、近期接种疫苗、存在已知的室内/室外污染物、暴露于诊断X射线以及以前的放射或化学疗法)。在Santa Marta进行初次面试期间一次采集了血液样本。在Boyaca,在初次采访时和1个月后抽取了血液样本。在Nariño、Putumayo和Valle del Cauca,在初次采访时与喷洒后五天内以及四个月后采集了血样。在淋巴细胞中,暴露前,具有微核的双核细胞(BNMN)在Santa Marta最低,在其余四个暴露区域相似。在第一次和第二次采样之间,Nariño,Putumayo和Valle del Cauca采集的血样显示具有微核的双核细胞(BNMN)有统计上显着增加。自我报告直接接触喷雾农田的受访者中,Nariño和Putumayo的平均BNMN较高,但差异无统计学意义。与暴露前和对照所有其他变量相比,多重线性回归表明暴露后所有四个暴露区域中BMNM的统计学显着增加(p <0.001)。与立即暴露后相比,暴露前立即平均BMNM值的最大总变化发生在Valle del Cauca,其中喷洒使用无需额外的佐剂草甘膦除草剂农达。
Kier(2015)[121]确定了另外16项关于农药使用的研究,其中包括一些草甘膦的接触。这16项研究中,有11项在所研究的人群中显示出一定程度的基因毒性,但没有将暴露主要归因于草甘膦,因此未将其纳入本综述。
总之,在三项研究中,在草甘膦喷洒区域对人体进行了基因毒性终点评估的两项研究中,有两项显示血液中DNA损伤的变化具有统计学上的增加。在最强的研究中,在喷洒前和喷洒后(<5天)检查个体的染色体损伤(微核)的三个区域显示出统计学上的显着增加。 在另一个区域,暴露后一个月测得暴露后的损伤,变化很小。
人类细胞的基因毒性(体外试验)
数项研究使用多种不同的方法检测了草甘膦在体外的基因毒性,这些细胞类型是来自喉癌、口腔癌、血液癌和肝癌的淋巴细胞、成纤维细胞和永生化细胞,并使用了几种不同的具有或没有代谢活化的基因毒性标记物。
Mladinicetal.(2009)[122]对暴露于浓度分别为3.5、92.8和580 µg / ml的三名健康人类供体的淋巴细胞(通过问卷排除基因毒性暴露)的草甘膦(未给出纯度)暴露引起的DNA链断裂(彗星测定)。对于没有S9激活的细胞,S9激活和锯切效果仅在最高剂量下发生。
Alvarez-Moyaetal.(2014)[123]进行了一项类似的研究,使用了人类志愿者的淋巴细胞(通过问卷排除基因毒性暴露)和浓度为0.12、1.2、12和120 µg / ml的草甘膦(纯度为96%)。所有暴露组均具有明显的剂量反应关系,而没有代谢激活(未测试代谢激活),发现DNA链断裂(彗星测定)显着增加。
Manasetal.(2009)[124]使用人类HEP-2细胞在676 µg / ml至1270 µg / ml之间所有浓度下,研究草甘膦(纯度为96%)诱导的DNA损伤(彗星测定)(未测试S9激活)。最高浓度下的细胞活力低于80%,未给出其他浓度下的值。
Monroyetal.(2005)[125]研究了草甘膦浓度(工业级,未提供纯度)范围为676 µg / ml至1000 µg / ml草甘膦中GM 38细胞诱导明显的DNA损伤(彗星测定),具有清晰的剂量反应模式。在相同的浓度范围内,他们还观察到所有剂量下细胞活力的浓度依赖性降低,这使得彗星试验结果难以解释。 在同一篇论文的类似分析中,使用纤维肉瘤HT1080细胞,他们发现了浓度依赖性DNA损伤和细胞活力丧失。 在两个实验中均未使用S9激活。
Luekenetal.(2004)[126]成纤维细胞GM 5757在浓度为12,680 µg / ml草甘膦(纯度为98.4%),并与40或50 mM H2O2接触可诱导DNA损伤(彗星测定)。 在本实验中未使用S9激活。这组作者说,在这种暴露水平下,细胞活力高于80%。
Kolleretal.(2012)[127]以浓度依赖的方式在浓度为20和40 µg / ml的草甘膦(> 95%纯度)下,显着诱导人TR146细胞(颊癌细胞)的DNA损伤(彗星测定)。高于40 µg / ml,相对于对照,尾巴强度有显着增加,但实际增加量并未随剂量增加而变化(平稳)。使用草甘膦除草剂农达(Roundup, Ultra Max)情况下,作者看到了在20和40 µg / ml时几乎相同的DNA损伤水平,但是浓度响应在暴露量以上继续增加。这些实验未使用S9激活。他们还使用同一系统中的CBMN分析来评估双核细胞中的微核总数(MNI)、带微核的双核细胞数(BN-MNI)、核芽数(NB)和核质数草甘膦和草甘膦除草剂农达(Roundup)暴露造成的核质桥(NPB)。浓度为10、15和20μg/ ml时,两个终点(NB,NPB)显着增加,浓度为15和20微克/毫升时,两个终点(MNi,BN-MNi)显着升高。等效的草甘膦除草剂农达暴露导致DNA损伤的所有四个测量值分别以10、15和20 µg / ml显着增加。草甘膦除草剂农达制剂的结果比单独使用草甘膦单一成分的结果更强。
Gasnieratal.(2009)[128]将来自肝癌细胞系HepG2的细胞暴露于草甘膦(未提供纯度)和四种草甘膦制剂中。仅测试一种草甘膦制剂的DNA损伤(彗星测定),当草甘膦当量浓度为0.05 µ / ml至4 µg / ml时,它们会产生显着影响(未给出p值)。没有提供p值,并且结果的表示并不能提供将这些结果与其他研究进行比较的明确方法。该研究将不会用于评估中。
Manas et al. (2009)[124]从三名健康的非吸烟女性和三名健康的男性中获取了人类血液样本,这些男性没有农药暴露史。用浓度分别为34、203和1015 µg / ml的草甘膦(纯度为96%)培养淋巴细胞,观察到的染色单体断裂、染色体断裂、染色单体间隙、染色体间隙、双着丝粒、无着丝粒片段或核内复制没有统计学上的显着变化。
Mladinic et al. (2009)[129]使用来自三名非吸烟健康志愿者的血液来评估微核、核芽和核质桥的形成与草甘膦(98%纯度)接触的关系。在S9激活的细胞中,以92.8和580 µg / ml的浓度服用草甘膦后,微核发生了显着变化,但没有代谢活化的细胞则没有。对于S9激活和未活化的细胞,核芽的变化均以580 µg / ml观察到,而在S9激活的细胞中,核浆桥的显着变化仅为580 µg / ml。该研究包含一个阳性对照(甲磺酸乙酯为200 µg / ml),在所有测定中均为阴性,多次显示其效果低于草甘膦。
Bolognesi et al. (1997)[130]从两名健康的女性供体那里获得血液,并将其暴露于草甘膦(纯度为99.9%)或抗农达制剂(草甘膦为30.4%)中。在浓度为1000、3000和6000 µg / ml的草甘膦以及浓度为100和330 µg / ml的草甘膦制剂中,姐妹染色单体交换(SCE)发生了显着变化。浓度为330 µg / ml时,仅草甘膦的SCE升高不明显,比农达制剂中等效草甘膦的暴露水平降低了约20%。这项研究没有考虑S9激活。
Lioi et al. (1998)[124, 131]从三位健康的供体者获取血液,将其暴露于草甘膦(纯度> 98%)。草甘膦的浓度分别为1.4、2.9和8.7 µg / ml时,观察到姐妹染色单体交换(SCE)和染色体畸变发生了显着变化。这项研究没有考虑S9激活。
Vigfusson and Vyse (1980)[132]将来自两个人培养的人类淋巴细胞暴露于浓度分别为250、2500和25000 µg / ml的草甘膦除草剂农达制剂(未知草甘膦%)。由于缺乏培养中的细胞生长,未提供最高浓度的结果。在一个供体中,其余两个浓度的姐妹染色单体交换(SCE)显着增加,而在另一个供体中,SCE的浓度最低。虽然本文中看到的相对SCE计数与Bolognesi et al. (1997)看到的结果类似,在这项研究中,控件中的绝对计数大约高出三倍。这项研究没有考虑S9激活。
非人类哺乳动物的基因毒性(体内)
Bolognesi et al. (1997)[130]通过腹膜内(IP)注射单次草甘膦(纯度为99.9%,300 mg / kg)或农达制剂(900 mg / kg,相当于270 mg / kg草甘膦草甘膦)暴露的三只瑞士CD-1雄性小鼠的暴露组。注射后4小时和24小时处死动物,除去肝脏和肾脏,从粘附的组织中获得粗核。对于草甘膦和农达,两个组织在四个小时的DNA单链断裂上均显示出显着增加(p <0.05),反应之间没有明显的差异。在24小时时,断链的存在减少了,并且与对照相比不再具有统计学意义。
Peluso et al. (1998)[133]将六只(对照组,草甘膦盐和农达制剂的最低剂量)或三只瑞士CD-1小鼠(雄性和雌性,未指定具体数目,肝和肾组织合并进行分析)暴露于异丙基铵、草甘膦盐或农达制剂(草甘膦的30.4%异丙基铵盐)处理24小时。在肝脏或肾脏中单独暴露于草甘膦盐的小鼠中,DNA加合物(标记后的32P-DNA)不明显,但在所有测试剂量的草甘膦除草剂农达制剂中均存在于肝脏和肾脏中,表现出剂量反应模式。
Rank et al. (1993)[134]通过腹膜内注射使雄性和雌性NMRI小鼠(每只雌性3至5只)暴露于草甘膦异丙胺盐(纯度未指定)和农达制剂(每升480 g草甘膦异丙胺盐)。 24或48小时后(对农达制剂仅限于24小时后),从骨髓中提取多色红细胞,并从1000个细胞的样本中对微核进行计数。在草甘膦暴露的动物(100、150和200 mg / kg)或在农达制剂暴露的动物(草甘膦当量剂量为133和200 mg / kg)中,任何浓度均未见明显增加。阳性对照尽管无统计学意义,但显示微核增加。
Bolognesi et al (1997)[130]通过三只、四只或六只雄性Swiss CD-1小鼠的腹膜内注射,以相等的剂量(间隔24小时)两次以草甘膦(纯度为99.9%)和农达制剂(草甘膦含量30.4%)暴露。在最后一次暴露后六到二十四小时后,从骨髓中提取多色红细胞,并从1000个细胞的样本中对微核进行计数。两次服用150 mg / kg草甘膦的小鼠在6小时时微核无明显增加,而在24小时时显着增加。相反,给予225 mg / kg草甘膦当量的农达制剂的两次剂量的小鼠在6小时和24小时都显示出微核的显着增加。草甘膦和农达制剂在24小时之间的微核平均绝对增加的相对差异(减去对照组的平均响应)为3.6,而草甘膦当量的相对差异为1.5,表明草甘膦制剂的效果更大。
Manaset al.(2009)[124]通过腹膜内注射,以相等于24小时的两次相等剂量将雄性和雌性Balb C小鼠组(未提供组大小,组织进行分析)暴露于草甘膦(纯度为96%)。暴露后二十四小时,从骨髓中提取多色红细胞,并从1000个细胞的样品中计数微核。在草甘膦暴露的动物中,剂量分别为50 mg / kg和100 mg / kg时,未见明显增加,但以400 mg / kg时,则有显着增加。阳性对照显示微核统计上显着增加(约为对照率的三倍)。
Dimitrov et al. (2006)[135]将八只雄性C57BL小鼠(组合用于分析的小鼠)通过灌胃以1080 mg / kg的剂量暴露于农达制剂(41%草甘膦)。在暴露后6、24、72、96或120小时,从骨髓中提取多色红细胞,并从4000个细胞的样品中计数微核(每只动物500个)。没有看到明显的增加。他们还寻找了这些动物的染色体损伤,没有发现明显的增加。阳性对照显示微核统计上显着增加。
Prasad et al. (2009)[136]通过腹膜内注射25和50 mg / kg剂量的15只雄性Swiss CD-1小鼠暴露于农达制剂(30.4%草甘膦)。在暴露后24、48或72小时,提取来自骨髓的多色红细胞,并从每只动物2000个细胞的样品中计数微核,每只动物五只动物。相对于对照,所有剂量下所有时间的微核计数均显着增加(p <0.05)。另外,在所有时间,所有剂量的具有染色体畸变的细胞数量均显着增加。微核的控制率与Bolognesi et al. (1997)的控制率相似,但剂量约小10倍时,其响应增加约50%。
Grisolia et al. (2002)[137]通过间隔24小时两次腹腔内注射(IP)以50、100和200 mg / kg的剂量农达制剂(480 g/每升草甘膦异丙胺盐)将瑞士小鼠(未提供性别和样本量)暴露于农达制剂。在暴露后24小时,从每只动物的2000个细胞的样品中提取来自骨髓的多色红细胞并计数微核。在任何剂量下微核计数均未增加。这种暴露似乎与Rank et al. (1993)研究中使用的农达制剂配方相同,结果也是负面的。
Coutinho do Nascimento and Grisolia (2000)[138]通过两次腹腔内注射(IP),分别以50、100和200 mg / kg的剂量将六只雄性小鼠(未给予品系)暴露于农达制剂(未给予草甘膦%)。在暴露后24小时,从每只动物1000个细胞的样品中提取来自骨髓的多色红细胞并计数微核。剂量为85 mg / kg时,微核显着增加。在42或170mg / kg剂量以下未见微核增加。
Cavusoglu et al. (2011)[139]通过单次注射草甘膦除草剂农达制剂(RoundupUltra Max,450 g /l 草甘膦,50 mg / kg草甘膦当量剂量)通过腹腔内注射(IP)暴露六只瑞士白化病小鼠。注射后三天处死动物。从每只动物1000个细胞的样品中计数正常色红细胞中的微核。红细胞中的微核显着增加(p <0.05)。G. bilboa消除了这些影响。
Chan and Mahler (1992)[140]将10只雄性和雌性B6C3F1小鼠的组,雄性以0、507、1065、2273、4776和10780 mg / kg的剂量暴露于草甘膦(纯度为98.6%),雌性为0,753、1411、2707、5846和11977 mg / kg,持续13周。处死时,从外周血中提取多色红细胞,并从10,000个细胞的样品中计数微核。在任何测试剂量下均未见明显增加。
Li and Long (1988)[141]通过腹膜内注射1000 mg / kg的剂量,将18只雄性和雌性Sprague-Dawley大鼠组暴露于草甘膦(纯度为98%)。在处理后6、12和24小时,处死每种性别的6只动物,并从骨髓中提取多色红细胞,并从每只动物50个细胞的样品中计数微核。暴露后任何时间点,具有染色体畸变的细胞百分比均未增加。
非人类哺乳动物细胞的基因毒性(体外试验)
LiandLong(1988)[141]将草甘膦(98%纯度)的中国仓鼠卵巢细胞(CHO-K1BH4)以5、10、50和100 mg / ml的浓度孵育了3小时。然后将每个样品一式三份地使用200个细胞铺板,并孵育8-12天。然后计数菌落,结果表示为突变频率。在有或没有S9激活的任何实验组中均未见阳性结果。目前尚不清楚为什么在该实验中各组的孵育时间有如此大的差异,也不清楚哪些组的孵育时间更长。在同一出版物的第二项研究中,未诱导的原代大鼠肝细胞(Fischer 344)与七种浓度的草甘膦(12.5 ng / ml至125 µg / ml)孵育18-20小时。在任何暴露浓度下,每个核的净谷粒均未见明显增加。最低暴露组相对于对照组增加了四倍,然后其他所有试验组均低于对照反应。这是一个非常不寻常的发现,可能是由于针对细胞质中的净颗粒调整数据的方式所致。作者通过从核数中减去最高的胞质数来计算每个核的净粒数;如果草甘膦增加了细胞质计数,这可能会偏向于发现,从而使核计数的任何增加都消失。没有提供数据来解决此问题。
Roustan et al. (2014)[142]将中国仓鼠卵巢细胞(CHO-K1)与草甘膦(未提供纯度)分别以2、5、10、15、17.5、20和22.5 mg / ml的浓度孵育3小时。然后将每个样品一式三份地使用200个细胞铺板,并孵育24小时。对于每种暴露浓度,检查2000个双核细胞的微核。在没有S9激活的任何实验组中均未见阳性结果,但是当存在S9激活时,四个最高暴露组显着,具有清晰的浓度反应模式。
Lioi et al. (1998)[131]将三只无关的健康母牛的淋巴细胞暴露于草甘膦(纯度> 98%)72小时,浓度为3、14.4和28.7 µg / ml,而没有激活S9。在所有草甘膦暴露浓度下,具有清晰的浓度反应模式,从150个细胞中获得的染色体畸变显着增加(P <0.05)。同样,每个细胞的SCEs在所有浓度下均增加(p <0.05),但没有明显的浓度反应模式。
Sivikova and Dianovsky (2006)[143]使用浓度分别为4.7、9.5、23.6、47.3、94.6和190 µg / ml的浓度使来自2只年轻公牛淋巴细胞暴露于草甘膦制剂(62%草甘膦)中,无S9激活。对于草甘膦的任何24小时暴露浓度(未进行2和48小时暴露),没有S9激活,从100个细胞获得的染色体畸变没有显着增加(P <0.05)。除最低浓度外,在所有24小时暴露浓度下(p <0.05),每个细胞的姐妹染色单体交换(SCE)均增加。在48小时时,在47.3 µg / ml或以上的浓度下,每个细胞的SCE显着增加(未进行2小时暴露)。最后,在暴露了S9激活情况下暴露2小时后,在5和10 µg / ml处观察到了显着的效果,而在15 µg / ml处没有观察到显着效果(S9激活未进行24和48小时暴露)。
Holeckova (2006)[144]将来自两只健康年轻公牛的淋巴细胞暴露于草甘膦制剂(62%草甘膦)中达24小时,浓度范围为28至1120 µmol / L,而没有激活S9。在56 µmol / L处观察到多倍体显着增加,所有其他比较均无显着性。但是,这一发现不容易被驳回,因为高于此浓度的所有暴露组的细胞数太少,无法进行评估。这项研究没有考虑S9激活。
非人类系统的基因毒性(体内和体外试验)
鱼类中的四项研究[123, 145-147]看到了草甘膦暴露后的基因毒性(DNA链断裂,不同的测定方法)的阳性结果。 此外,一项针对牡蛎精子和暴露于草甘膦的胚胎的研究[148]并未发现DNA损伤的增加(彗星分析),而针对两种果蝇的一项研究[149]则表明突变在更高剂量暴露中有所增加(翼点试验)。。
在多种鱼类中进行的十四项研究[137, 145, 147, 150-160]评估了各种草甘膦制剂与基因毒性之间的关系,所有研究均显示了各种终点(DNA链断裂、微核形成和染色体畸变)阳性结果。其中两项研究[150, 152]对接触草甘膦制剂后的微核形成显示阴性,其中一项研究[150]对染色体畸变也显示阴性,但是在其他遗传毒性标记中均为阳性。两项研究[161, 162]证明了体内接触草甘膦制剂对凯门鳄具有基因毒性(DNA链断裂、微核)。三项研究[163-165]证明了暴露于草甘膦制剂中的青蛙或蝌蚪显示基因毒性(DNA链断裂、微核形成)。对牡蛎精子和胚胎的一项研究[148],与对蛤蜊的一项研究[166]和贻贝暴露于草甘膦制剂一项研究[167]没有发现DNA损伤的增加(彗星分析)。一项关于蜗牛的研究[168]发现,接触草甘膦制剂后DNA损伤增加(彗星分析)。蠕虫中的两项研究[169, 170]看到了DNA损伤的混合结果(彗星测定),其中一项研究[169]显示了微核形成的阳性结果。一项关于果蝇的研究[171]显示,性相关的隐性致死突变增加。
在已发表的文献中,有五项研究评估了草甘膦在体外系统中的影响。其中两项研究[172, 173]研究了草甘膦与户外紫外线辐射(UVB)辐射一起的基因毒性,发现未代谢激活的细菌的DNA链断裂(FADU分析)显着增加。一项关于真核生物鱼的研究[174]看到没有激活S9的DNA链断裂(彗星测定)显着增加。另一项研究[141]显示,在有S9激活和没有S9激活的两种细菌中,反向突变均没有增加。
Williams et al. (2000)[175]总结了在鼠伤寒沙门氏菌中使用反向突变测定法的文献(艾姆斯试验)。使用草甘膦的四项研究和草甘膦制剂的五项研究均为阴性。他们引用了一项关于草甘膦制剂的研究[134],该制剂在S9激活时为阳性,而在没有S9激活时为阴性。但是,这项研究在TA100细胞中对S9激活呈阳性,在TA98细胞中对S9激活呈阴性,对于TA100细胞不具有S9激活呈阴性,而对于TA98细胞不具有激活是阳性。他们还总结了大肠杆菌(e. coli)中草甘膦的两项研究,带有和不带有激活均为阴性。
科学文献中还提供了另外两项使用反向突变测定法检测草甘膦的研究[141, 176],两者均为阴性。
监管机构举证的研究(Regulatory Studies)
欧洲食品安全机构(EFSA)[89]引用了鼠伤寒沙门氏菌中的14种反向突变测定(Ames试验),其中大多数在TA 98、100、1535、1537菌株中进行了测试(表B.6.4-1)。 EFSA将所有14项研究列为阴性。仅提供了14项研究中的一项的实际数据,该研究显然是阴性的。 美国环保署(EPA)[61]引用了鼠伤寒沙门氏菌中的27种反向突变测定法(Ames试验),其中大多数在TA 98、100、1535、1537菌株中进行了测定(EPA表5.1)。所有27项研究均被列为阴性。没有提供任何研究的数据。Kier and Kirkland (2013)[177]引用了草甘膦对18种细菌反向突变测定结果和16种草甘膦制剂测定的结果。提供了所有34项研究的列表结果和背景信息。六项研究在仅草甘膦的一个或多个组中显示出阳性结果。
欧洲食品安全机构(EFSA)[89]引用了三项关于哺乳动物细胞基因突变的研究,全部被列为阴性(EFSA表B.6.4-5),两项使用小鼠淋巴瘤测定,另一项使用中国仓鼠卵巢细胞/次黄嘌呤-鸟嘌呤-磷酸核糖基转移酶(CHO / HGPRT)突变测定。 美国环保署(EPA)[61]引用了四项研究,其中三项似乎与EFSA引用的研究相同(EPA表5.2),第四项是另一项小鼠淋巴瘤测定。所有这四个列为阴性。Kier and Kirkland (2013)[177]引用了两项小鼠淋巴瘤研究并提供了列表数据。两项研究均未显示L5178小鼠淋巴瘤tk(+/-)细胞的胸苷激酶基因座突变频率有统计学显着增加的迹象。
欧洲食品安全机构(EFSA)[89]引用了一项关于哺乳动物细胞中DNA损伤和修复的体外研究,该研究被列为阴性(EFSA表B.6.4-6)。这项研究涉及原代大鼠淋巴细胞的计划外DNA合成(UDS分析)。他们还列出了五项染色体畸变研究(EFSA表B.6.4-8),这些研究被定性为阴性。两项研究涉及人类淋巴细胞,两项研究涉及中国仓鼠肺(CHL)细胞。 CHL中一项研究的数据以表格形式提供,显然是负面的。 美国环保署(EPA)[61]引用了八项关于哺乳动物细胞染色体畸变的体外研究(EPA表5.3);其中两项研究与EFSA报告中的研究相符。其中四项研究来自文献[124, 131,143,178],并对其进行了综述。令人惊讶的是,EPA指出Manas et al. (2009)[124]显示阴性,尽管在彗星试验中明显为阳性。此外,EPA称Sivikova and Dainovsky (2006)[143]的研究为阴性,即使他们看到草甘膦对姐妹染色单体交换(SCE)的影响明显。基本上,EPA引用的所有四项文献研究均为阳性,但EPA仅列出了四项中的两项为阳性。EPA引用的其余四项研究均为阴性。但是没有提供这些研究的数据。Kier and Kirkland (2013)[177]引用了八篇文献研究(均在上文中进行了综述)和三篇有关草甘膦暴露的监管引用研究。这三项法规研究被列为阴性,数据可作为Kier and Kirkland (2013)的补充材料中的表格获得。这些研究在CHL细胞中所有测试浓度下均为阴性;一个与EFSA提供的研究数据相匹配[89]。
欧洲食品安全机构(EFSA)[89]引用了9种微核检测方法,其中3种在瑞士的Albino小白鼠中进行,两个在NMRI小鼠中进行,两个在CD-1小鼠中进行,一个在SD大鼠中进行,另外一个在CD大鼠中进行(EFSA表B.6.4-12)。他们列出了瑞士白化病小鼠的一项研究在雄性中为弱阳性,在CD-1小鼠中的一项研究在最高剂量下为阳性(提供了该研究的数据),所有其他研究均为阴性。他们放弃了一项对低剂量雄性瑞士小鼠的研究,但为该研究提供的表格显示,在使用最高剂量(30 mg / kg)显示明确的剂量反应时。他们提供了两项阴性研究的数据,这些数据表明这些研究确实是阴性的。 美国环保署(EPA)[61](EPA表5.5)引用了20种微核化验,其中4篇为可以访问科学文献,而3篇已在上面进行了评论(在撰写本报告时,我尚无第四篇参考文献[179])。其余的16项研究包括在瑞士白化病小鼠中进行的6项研究、在CD-1小鼠中进行的4项研究、在NMRI小鼠中进行的3项研究、在Sprague-Dawley大鼠中进行的两项研究以及在Wistar大鼠中进行的一项研究。由于EFSA没有提供与其微核研究相关的名称,因此我无法确定EPA引用的任何研究是否与EFSA引用的研究相同。 EPA列出了两项文献研究为阳性,两项为阴性(与我对我所获得的三项研究的评价相符),而除一项监管机构引用研究以外,其余均为阴性(一项对瑞士白化病小鼠的阳性研究)。 Kier and Kirkland (2013)[177]引用了12种草甘膦的监管微核试验,并提供了全部12种的数据表。所有12项研究均被EPA引用。 Kier and Kirkland (2013)列出11项研究为阴性,一项没有结论。但是,其中有四项研究显示了至少一个按性别列出的试验组具有阳性作用。他们将这四项研究中的一项列为无定论,而其余三项研究被确定为阴性,因为反应在历史控制范围内。正如针对动物致癌性研究所讨论的那样,正确使用的组是对照组。
Kier and Kirkland (2013)[177]也引用了12项监管研究和3篇文献研究,其中动物接触的是草甘膦制剂。上面回顾了两项文献研究,而其余研究[179]无法获得。 Kier and Kirkland (2013)在表中提供了12项调控研究的数据,并显示了CD-1小鼠的两项阳性研究和其余10项的阴性研究。
基因毒性总结(Summary for Genotoxicity)
由于现有研究的多样性,这是一个很难得出结论的复杂领域(有多个物种、一个物种中的多个菌株、来自多个物种的多种细胞类型、不同的暴露时间长度、不同的暴露后评估时间、不同的暴露、大量的基因毒性标记,最后是草甘膦和多种不同的草甘膦制剂)。有三项研究直接评估草甘膦对人体的基因毒性;八种小鼠品系中36项实验;大鼠中的三项研究;人类淋巴细胞中的九项研究、其他人类细胞中的四项研究;非人类哺乳动物细胞系中的12项研究(2项使用小鼠细胞,5项使用仓鼠细胞,2项使用大鼠细胞,3项使用牛细胞),针对多种非哺乳动物物种的大量研究,以及对细菌的大量研究,大多数是相同的。
一些结论直截了当;“草甘膦似乎不会引起鼠伤寒沙门氏菌中组氨酸合成的反向突变,无论这些反向突变是由于移码突变还是由于点突变引起的”。我对这一决定持谨慎态度,因为有几项研究取得了阳性的结果,但没有明显的规律可循。有足够的证据支持这一结论,即草甘膦制剂和草甘膦可引起非哺乳动物动物的基因毒性。这清楚地表明草甘膦和制剂均能引起DNA损伤。因此,尽管这些物种的基因毒性发现不能直接说明对人类的潜在危害,但它们确实令人担忧。
更重要的研究是使用哺乳动物系统、人类细胞和人类直接接触进行的研究。表17在一个简单的框架中总结了这些研究,使您一眼就能看到所有实验数据。该表未解决解释任何一项研究所需的精妙之处,仅说明了一项研究何时产生阳性结果还是阴性结果。
显然,对于人体细胞的体外试验评估,大多数研究已产生了阳性结果。只有一项监管研究评估了健康志愿者的人淋巴细胞中草甘膦的基因毒性,但该研究结果为阴性。该研究与该类别中的其他六项研究没有显着差异,其中五项产生了阳性的结果。这些研究中的大多数都使用彗星测定法(一种测量任何类型的DNA链断裂的简单方法)或计算细胞中特定类型链断裂的方法(例如SCE,微核,核芽和核质桥)。从这些测定中,我们可以得出结论,存在DNA损伤。对于草甘膦制剂,在人体体内只有三项研究,其中两项是阳性的。
如果草甘膦在细胞中引起细胞毒性,则在这些研究中使用的浓度大小可能会导致假阳性。使用彗星试验的所有六项研究均为阳性,没有研究显示低于10 µg / ml的阴性反应,低于结果的混合结果低于0.12和3.5 µg / ml的阳性结果,而阴性结果为2.91和10 µg / ml的阴性结果。通常,彗星试验为基因毒性提供了有力的支持。
直接研究了草甘膦暴露后细胞中特定类型的链断裂的四项研究表明,在所使用的各种浓度下,其反应明显不同。Manas et al. (2009)在3.4-1015 µg / ml的浓度范围内,染色单体断裂、染色体断裂、染色单体间隙、染色体间隙、双着丝粒、无着丝粒片段或核内复制没有变化。相反,Lioi et al. (1998)看到姐妹染色单体交换(SCE)在1.4至8.7 µg / ml范围内变化。
两项研究均在志愿者的淋巴细胞中进行。Mladinic et al. (2009)在高于92.8微克/毫升时看到微核的重大变化,Bolognesi et al. (1997)在高于1000 µg / ml时看到的SCEs发生了阳性的变化,但在330 µg / ml时没有变化。尽管四项研究中的三项中都观察到了变化,但是在研究中发现变化的实际浓度并不一致。我得出的结论是草甘膦会导致DNA链断裂,这表明它具有基因毒性。
除CD-1小鼠中的三项研究和瑞士白化病小鼠中的四项研究外,检查草甘膦基因毒性的啮齿类动物中的微核测定要么全部为阳性,要么在一种品系中全部为阴性。对于阳性研究,我们可以问这个品系中微核的实际数目是否一致的问题。
表17:草甘膦和草甘膦制剂在哺乳动物中的体内和体外基因毒性研究摘要1
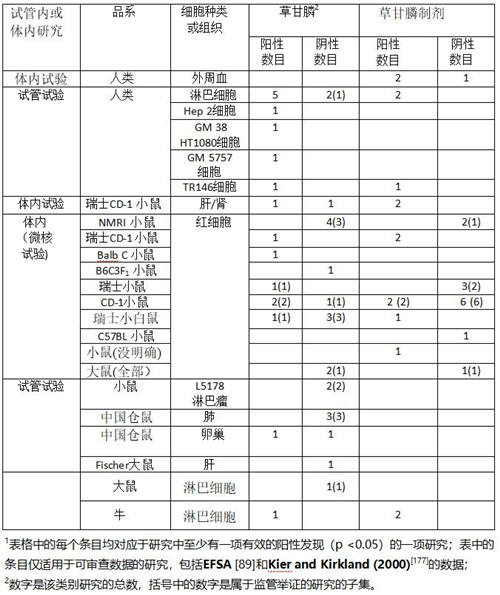
在瑞士小白鼠中,所有四项研究均以雄性和雌性进行。阳性研究(雌性小鼠)通过口管暴露,阴性研究通过腹腔内注射(IP)。阳性研究的剂量为5000 mg / kg,而任何阴性研究的最高剂量均为3024 mg / kg。最后,阳性研究中的对照反应为每1000 PCE 6.7微核PCE,而三个阴性研究中的对照则为每1000 PCE 0到0.6微核PCE。这些差异中的任何一个都可以轻松解释应答的差异,因此应接受瑞士小白鼠的阳性结果。
对于CD-1小鼠,一项阴性的微核研究是通过以5000 mg / kg的单剂量口服灌胃雄性和雌性。一项阳性的研究还通过对雄性口服管饲,剂量为2000 mg / kg。由于统计噪声的性质,无论是否存在真正的影响,这两项研究都可能同时发生。对于另一项阳性研究,该剂量是通过腹腔内注射(IP)在雄性小鼠中产生的,其阳性反应为600 mg / kg,是对照反应的两倍以上。这些数据支持了草甘膦可以在雄性CD-1小鼠中引起微核的发现,这表明了基因毒性。
暴露于草甘膦的哺乳动物细胞中的其余体外测定显示出不同的结果。小鼠淋巴瘤测定法和中国仓鼠卵巢测定法正在寻找可使这些细胞在培养物中生长的特定突变。中国仓鼠肺,两只大鼠测定法和牛淋巴细胞测定法正在测量DNA损伤并提供混合结果。通常,这些反应似乎是阴性的,但在牛淋巴细胞中所见的反应似乎与草甘膦接触后SCE呈正增加。
对于草甘膦制剂,草甘膦发现与草甘膦制剂发现之间的主要区别是人类基因毒性的直接证据和瑞士小鼠的微核化验。在总体分析中,观察到草甘膦制剂对人体的基因毒性观察必须承担最大的权重,而三项研究中有两项是阳性的,Bolognesi et al. (2009)[120]的研究权重最强,显示出最强烈的反应。
对于瑞士小鼠的微核研究,三项研究均对草甘膦制剂呈阴性,而一项研究对草甘膦呈阳性,这一事实造成了明显的分歧。呈阳性的研究是一项管饲法研究,在雄性小鼠中以30 mg / kg /天的剂量观察到了这种作用。草甘膦制剂的两项阴性引证监管研究均以2000 mg / kg(约500 mg / kg草甘膦当量)进行,也是口服管饲研究,并且是在同一实验室在不同时间进行的重复试验。其余的阴性研究使用的草甘膦制剂剂量为50-200 mg / kg(相当于草甘膦的25-100 mg / kg),但通过腹膜内注射进行。除了不同的接触途径外,这些研究之间的差异无法解决。
在这种情况下,不可能对数据进行汇总分析,因为几乎在每种情况下,没有一项研究可以清楚地复制另一项研究。相反,适当的方法是进行荟萃分析,并评估实验设计的哪些方面对产生基因毒性的积极发现很重要。这类分析数据最多的研究是微核形成的各种体内测定。 Ghisi et al. (2016)[180]进行了系统搜索,以鉴定所有评估草甘膦或草甘膦制剂在体内诱导微核的能力的已发表研究。作者还使用了上文总结的Kier and Kirkland (2013)[177]的数据。在评估中,一项实验是根据草甘膦的性别/种类/途径/形式定义的,因此一些使用草甘膦和草甘膦制剂进行两性研究的研究将多次进入分析。他们确定了93个可以进行荟萃分析的实验。提取每项研究的数据,每个实验组的平均值与平均对照反应(E +)的对数比用于评估荟萃分析中的效应大小。对于此荟萃分析平均值,低于零的值表示无基因毒性,而高于零的值表示基因毒性增加。还评估了异质性测试(前面针对流行病学数据讨论的Cochran Q统计量)。
图2拷贝自Ghisi et al. (2016)[180]研究的图1,是他们评估的所有草甘膦和草甘膦制剂研究的森林图(forest plot)。 从该图可以清楚地看出,这些数据中的主要反应为阳性,所有研究E+=1.37的总体总体均值反应和(1.356-1.381)的95%置信区间(在ap <0.0001时具有统计学意义 )。 总体平均值的Qt值在统计上也很有意义,表明数据中还有其他解释变量可以帮助解释总体差异。
然后使用分类变量对数据中的各个层次进行比较,以确定哪些实验条件对平均响应的影响最大。哺乳动物物种的平均效应(E+=1.379; 1.366-1.391)比非哺乳动物物种(E+=0.740; 0.641-0.840)更高。草甘膦制剂的平均响应(E+=1.388; 1.375-1.400)比草甘膦(E+= 0.121; 0.021-0.221)大,但两者均显着大于零。仅使用雄性动物(E+= 1.833; 1.819-1.847)的研究中的平均应答与使用雄性和雌性的动物(E+= 0.674; 0.523-0.825)的零应答显着不同,而仅使用雌性动物的研究(E+0.088;-0.153-0.328)不是。与监管引证研究(E+=0.114; 0.027-0.202)相比,经过同行评议的研究具有更高的平均应答率(E+=1.394; 1.381-1.407),但两种方法均显着大于零,表明总体基因毒性作用。还检查了其他变量,例如暴露时间长短和暴露量,对总体发现影响很小.
Ghisi et al. (2016)[180]的荟萃分析为以下假说提供了有力的支持:草甘膦和草甘膦制剂的接触会增加体内微核的形成。 这意味着草甘膦和草甘膦制剂正在破坏具有完整DNA修复能力的功能正常的生物体内的DNA,从而加强了草甘膦对人类基因毒性的发现。
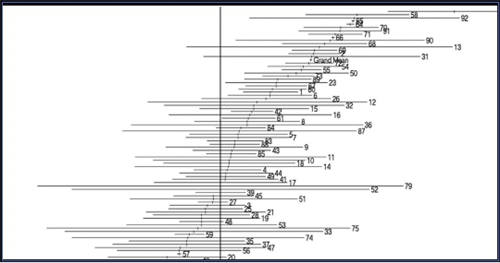
图2:评估草甘膦暴露中微核频率的研究的森林图,按效应大小排列。 该图显示了荟萃分析中每个实验的响应率和95%置信区间(CI)的估计值。条旁的数字代表每个实验的参考数字,如Ghisi et al. (2016)[180]的表1中所示。均值是所有研究的总体均值效应大小。 [转载自Ghisi et al. (2016)[180]]
从简单的统计角度来看,还有另一种方法可以决定小鼠微核试验中的阳性结果是否偶然。对于草甘膦研究,如果将所有单个实验组加起来,总共有79个组,对应于79个统计测试。假设所有测试的关键测试水平为0.05,则希望看到不到四个阳性的发现,但观察到六个。对于草甘膦制剂,有70个实验组,因此人们期望3.5个阳性结果,但观察到12个(p <0.01)。总体而言,在小鼠中总共检查了149个实验组的微核形成,我们观察到了18个(预期值为7.5,p <0.01)。在研究而非实验组的基础上重复此分析,有15项关于草甘膦的研究(预期数目为0.75阳性),但观察到6份阳性(p <0.01)。对于草甘膦制剂,有18项研究(预期数量为0.9阳性),但观察到6项阳性(p <0.01)。现在扩展到表17中列出的所有69项研究,有33项阳性研究,但预期仅为3.5(p <0.01)。
显然,草甘膦和草甘膦制剂均具有遗传毒性潜力。但是哪个更糟?在表17中的69个实验中,有五个来自五个研究出版物的实验,它们在同一实验室中研究了草甘膦和草甘膦的配方。其中,有两个对草甘膦和制剂均呈阴性,对讨论相对效价没有帮助。其余六个可以为草甘膦相对于草甘膦制剂的相对效力提供一些指导。Koller et al. (2007)[127],将草甘膦制剂中的草甘膦的量与仅使用相同量单一成分草甘膦的结果进行比较时,彗星试验的尾部强度几乎相同。在同一篇论文中,草甘膦制剂中的微核和相关生物标记始终高出10-20%。在Bolognesi et al. (1997)[130],在等剂量的草甘膦和草甘膦制剂下,瑞士CD-1小鼠肝脏和肾脏的DNA链断裂实际上是相同的。在他们的微核试验中,草甘膦制剂的效力高出约50%。最后,Bolognesi et al. (1997)[130],在他们对人淋巴细胞中SCE的分析中,草甘膦制剂的效力大约是单独草甘膦的两倍。在Peluso et al. (1988)[133],仅在服用草甘膦制剂的小鼠中观察到肝脏和肾脏中的DNA加合物,因此这些发现不太可能归因于草甘膦。数据表明,相对于单独使用草甘膦会看到的基因毒性,草甘膦制剂产生基因毒性的可能性有所增加。
总而言之,数据支持了草甘膦和草甘膦制剂均具有基因毒性的结论。 因此,支持人和动物中由草甘膦和草甘膦制剂引起的肿瘤增加存在合理的机制。
氧化应激(Oxidative Stress)
氧化应激是指细胞中活性氧物质(自由基)的产生与细胞为防止这种情况而应有的抗氧化剂防御之间的不平衡。氧化应激已与包括癌症在内的多种疾病[181-186]的起因和后果相关联[37,187-191]。存在多种用于氧化应激的生物标记。最常见的是增加抗氧化酶活性、减少谷胱甘肽或增加脂质过氧化作用。此外,许多研究通过接触草甘膦后使用抗氧化剂来证明氧化应激的作用可以减弱来评估氧化应激。
人细胞中的氧化应激(体外试验)
Mladinic et al. (2009)[122]研究了三名健康人类供体(使用问卷调查法排除其他基因毒性暴露)的淋巴细胞接触浓度为0.5、2.91、3.5、92.8和580微克/毫升的草甘膦(纯度为98%)对氧化应激的诱导。对于具有S9激活和不具有S9激活的细胞,总的抗氧化能力仅在未进行S9激活的细胞中以最高剂量增加,尽管在使用S9激活的情况下可以看到清晰的浓度响应模式。
Kwiatkowska et al. (2014)[192]研究了从波兰Lodz血库的健康捐献者那里获得的红细胞暴露于草甘膦(未给出纯度)对氧化应激的诱导作用。红细胞暴露于1.7、8.4、17、42.3、85和845 µg/ml的浓度,并孵育1小时。氧化应激(二氢若丹明123的氧化)在42.3、85和845 µg/l时明显增加,并具有清晰的浓度响应模式。
Chaufan et al. (2014)[193]研究了在HepG2细胞(人肝癌细胞系)中接触草甘膦(纯度为95%)和草甘膦除草剂农达(Roundup UltraMax)(草甘膦为74.7%)对氧化应激的诱导作用。草甘膦的暴露浓度为900 µg / ml,草甘膦制剂的暴露浓度为40 µg / ml。孵育24小时后,暴露于草甘膦制剂(增加了SOD活性)诱导了氧化应激(表示为超氧化物歧化酶(SOD)、过氧化氢酶(CAT)、谷胱甘肽(GSH)和谷胱甘肽S-转移酶(GST)的活性)显着增加(p <0.0-5),但单独使用草甘膦没有诱导。
Coalova et al. (2014)[194]研究了Hep-2细胞(人上皮细胞系)暴露于草甘膦制剂(Atanor,48%草甘膦)或表面活性剂(Impacto)对氧化应激的诱导作用。对草甘膦制剂(Atanor)的暴露浓度为376.4 µg / ml,对表面活性剂(Impacto)的暴露浓度为12.1 µg / ml,对两者混合物的暴露浓度为180.2 µg / ml。孵育24小时后,Impacto,Atanor及其混合物诱导的氧化应激(以SOD,CAT,GSH和GST的活性衡量)显着增加(仅CAT和GSH,p <0.05或p <0.01)。
Gehin et al. (2005)[195]研究了HaCaT细胞(人角质形成细胞系)暴露于草甘膦(纯度未知)和草甘膦制剂(Roundup 3 plus,21%草甘膦)引起的氧化应激。草甘膦诱导的细胞毒性被抗氧化剂减少或消除。作者将细胞毒性归因于氧化应激。
Elie-Caille et al. (2010)[196]研究了HaCaT细胞(人角质形成细胞系)中草甘膦(纯度未知)的暴露对氧化应激的诱导作用。暴露浓度范围从1700 µg / l到几乎12,000 µg / ml。草甘膦诱导细胞毒性并增加过氧化氢过氧化氢(二氯二氢荧光素二乙酸盐测定)。这项研究使用了异常高的浓度,该浓度可能独立于观察到的氧化应激而诱导细胞毒性,但用二氯二氢荧光素二乙酸盐测定法测定氧化应激有局限性[197,198]。
George and Shukla (2013)[199]研究了HaCaT细胞(人角质形成细胞系)暴露于草甘膦制剂农达(Roundup Original,41%草甘膦)引起的氧化应激。暴露浓度范围为1.7 µg / ml至17,000 µg / ml,暴露时间为24小时。草甘膦在所有浓度下均以浓度依赖的方式显着诱导了活性氧的形成(二氯二氢荧光素二乙酸盐测定)。用N-乙酰半胱氨酸预先处理细胞可以降低草甘膦的影响,但不能消除。用二乙酸二氯二氢荧光素测量氧化应激有局限性[197,198],影响了对这些结果的清晰理解。
非人类哺乳动物体内的氧化应激(体内试验)
Bolognesi et al. (1997)[130]通过腹膜内注射(IP)单次剂量的草甘膦(纯度为99.9%,300 mg / kg)或制剂农达(900 mg / kg,相当于270 mg / kg草甘膦)对三只瑞士CD-1雄性小鼠进行暴露。注射后8小时和24小时处死动物,除去肝脏和肾脏,从粘附组织中获得粗核。对这些小鼠的肝和肾样品进行了8-羟基-2'-脱氧鸟苷(8-OHdG)水平的评估,该水平是氧化应激的生物标记[200]。在草甘膦暴露后24小时,肝脏中的8-OHdG有显着增加,但在8小时时则没有,在肾脏中也没有。在8小时和24小时时,农达制剂均增加了肾脏中的8-OHdG,但在24小时时肝脏中所见的轻度升高并不明显。
Cavusoglu et al. (2011)[139]通过腹膜内注射(IP)草甘膦制剂农达制剂(RoundupUltra Max,450 g / l草甘膦,50 mg / kg制剂)暴露了六只瑞士白化病小鼠。给药结束时,将动物禁食过夜,然后处死。暴露于草甘膦制剂后,肝脏和肾脏中的丙二醛显着增加,肝脏和肾脏中的GSH显着降低。银杏叶(G. bilboa)消除了这些影响。【银杏叶具有抗氧化作用--译注】
Jasper et al. (2012)[201]通过口服管饲草甘膦制剂(Roundup Original,41%草甘膦,50 mg / kg草甘膦当量),将每组10只雄性和10只雌性瑞士白化病小鼠暴露15天。注射后三天处死动物。两种剂量下的雄性和雌性小鼠肝脏中的硫代巴比妥酸反应性物质(TBARS)均显着增加(p <0.05)。在两个剂量组中,雄性和雌性动物中硫醇的浓度均升高(雌性中尽在高剂量升高)(此终点未见剂量反应)。
Astiz et al. (2009)[202]通过腹膜内注射单剂量草甘膦(纯度未知,10 mg / kg)暴露了四只雄性Wistar大鼠组。每周给动物注射三遍,共五周,然后处死。对硫代巴比妥酸反应性物质(TBARS测定)、蛋白羰基(PCOS)、总谷胱甘肽水平、个体谷胱甘肽水平、SOD和CAT均作为血浆、脑、肝和肾中氧化应激的生物标志物进行了测量。草甘膦显着提高所有组织中的TBARS(p <0.01)、脑中总谷胱甘肽(p <0.01)、肝和脑中SOD(p <0.01)和脑中CAT。在一个追踪报告[203]中,他们证明硫辛酸消除或严重减少
草甘膦对大脑的影响。
Cattani et al. (2014)[204]在妊娠第5至15天的饮用水中,以41.4毫克/千克的剂量使四只怀孕的Wistar大鼠组暴露于草甘膦制剂(Roundup Original,360 g / L草甘膦)中。检查了15天大的幼崽(每只大坝2只)中海马的氧化应激标记。幼仔的TBARS显着增加(p <0.05),GSH显着降低(p <0.01)。
George et al. (2010)[82]通过单次局部应用,将四只瑞士白化病小鼠小组暴露于剂量为50 mg / kg(草甘膦当量)的草甘膦制剂(Roundup Original,36g / L草甘膦)。从接受试验的动物皮肤进行蛋白质组学分析后,发现SOD1、CA III和PRX II发生了变化,这些蛋白在氧化应激的管理中起着重要作用。
非哺乳动物系统中的氧化应激(Oxidative Stress in Non-Mammalian Systems)
对于基因毒性,Slaninova et al. (2009)[205]对回顾综述了对各种水生生物接触草甘膦和草甘膦制剂引起的氧化应激进行的研究。Slaninova et al. (2009)回顾的许多研究显示了草甘膦与各种器官的氧化应激的关联。 自从该综述以来,已经完成了其他研究,这些研究也证明了草甘膦与氧化应激之间存在阳性相关[147,156-159,206-217]。
氧化应激总结(Summary for Oxidative Stress)
七项研究针对人类细胞中的氧化应激,另外六项研究针对哺乳动物系统中的氧化应激。在来自健康供体的淋巴细胞和红细胞中,氧化应激在淋巴细胞中在低至580 µg / ml暴露中发现,在红细胞中低至42.3 µg / ml暴露中发现。在Hep-G2细胞中,单一浓度为900 µg / l时,氧化应激没有增加。在HaCat细胞的两项研究中,草甘膦在连续模型中诱导的氧化应激与一项研究的结果相符,而在另一项研究中仅与浓度最低(1700 µg / ml)的结果相符。关于人体细胞中氧化应激的最令人信服的研究是人体血液中的两项研究。
在瑞士CD-1雄性小鼠中,在注射300 mg / kg草甘膦后的24小时,但不是在4小时后,在肝脏中发现氧化应激增加。肾脏中未见增加。在Wistar大鼠中,使用多种生物标记物反复使用草甘膦进行腹腔内注射(IP)给药会导致多个器官的氧化应激增加。因此,所有的实验室研究均表明氧化应激在大鼠研究中具有重要意义。
在Hep-G2细胞中,草甘膦制剂显示出暴露于40 µg / ml的氧化应激显着增加。考虑到该细胞系中仅草甘膦的阴性反应,必须得出结论,该反应不是由于草甘膦引起的。在HEP-2细胞中,草甘膦制剂通过多种生物标记物以376 µg / ml的浓度显示了氧化应激的强劲增加,而添加表面活性剂时以180.2 µg / ml的浓度显示了氧化应激的强烈增加。在HaCaT细胞中,从低至1.7 µg / ml的剂量开始,草甘膦制剂以浓度依赖的方式显示出氧化应激的显着增加。没有关于人类淋巴细胞的研究。
在瑞士CD-1小鼠中,草甘膦制剂可显着增加肾脏的氧化应激,但仅显示肝脏轻度(无明显)增加。这项研究评估了暴露后两个不同时间点的氧化应激,并观察到了随时间变化的响应。草甘膦而不是草甘膦制剂在肝脏中造成的强烈增加,表明纯草甘膦相对于制剂的复杂响应模式可能与接触后的时间有关。在瑞士的白化病小鼠中,草甘膦制剂通过肝脏和肾脏中两个单独的生物标记物表现出增加的氧化应激。在使用不同生物标志物但剂量相似的瑞士白化病小鼠的第二项研究中,在肝脏和肾脏中均发现氧化应激增加。在暴露于子宫内的Wistar大鼠幼崽中,在海马体中发现了氧化应激的增加。在瑞士的白化病小鼠中,草甘膦制剂在皮肤上的局部应用导致蛋白质组指纹图谱的出现,表明氧化应激增加。
尽管对氧化应激的研究少于对基因毒性的研究,但在人类细胞和啮齿动物研究中看到的强烈反应清楚地支持了草甘膦和草甘膦制剂在诱导氧化应激中的作用。因此,存在第二种合理的机制,通过该机制,草甘膦和草甘膦制剂可引起人和动物中见到的肿瘤。
生物合理性摘要(Summary for Biological Plausibility)
在对因果关系的评估中,生物学上的合理性证据是压倒性的。 草甘膦显然会引起小鼠多种癌症,造血系统中的两种癌症与人类所见相似,会导致大鼠癌症,具有基因毒性并诱发氧化应激。 对于单独的草甘膦和草甘膦制剂,该发现都是清楚的。 对于草甘膦和草甘膦制剂与非霍奇金淋巴瘤(NHL)因果关系的支持,强烈支持生物学上的合理性。
生物梯度(Biological Gradient)
仅有三项流行病学研究在其出版物中提供了有关生物梯度的信息。
Eriksson et al. (2008)[46]将他们的病例和对照分为每年暴露≤10天和每年暴露> 10天的病例和对照。使用多变量分析计算OR,其中包括OR统计学上显着增加或OR> 1.50且至少有10名暴露受试者的药物。草甘膦的OR每年≤10天为1.69(0.70-4.07),每年> 10天为2.36(1.04-5.37)。在他们的多元分析中,潜伏期为1-10年的OR为1.11(0.24- 5.08),> 10年的OR为2.26(1.16-4.40)。因此,它们显示出随着暴露强度和潜伏时间的增加。
McDuffie et al. (2001)[50],使用条件对数回归分析控制农药的主要化学类别和所有其他协变量,且p <0.05,每年暴露≤2天的OR为1.0(0.63-1.57),≥2每年的天数,OR为2.12(1.20-3.73)。因此,它们显示出随着曝光强度的增加。
De Roos et al. (2005)[45]在分析中使用了三种暴露指标:a)曾经亲自混合或使用过的含有草甘膦的农药; b)草甘膦的累积接触天数(使用年数乘以每年的天数); c)强度加权的累积暴露天数(使用年数乘以每年的天数乘以使用强度)。对于b和c暴露量测量,他们将受访者分为先验选择的三分位数,以避免在处理稀有肿瘤时缺乏稀疏数据。对于累积暴露天数并使用最低暴露的三分位数作为参考组,针对人口和生活方式因素以及其他农药分别调整的三分位数2和3的RR分别为0.7(0.4-1.4)和0.9(0.5-1.6)。 30,699个主题)。当检查强度加权暴露天数时,分别针对人口和生活方式因素以及其他农药(30,699名受试者)进行调整的三分位数2和3的RRs分别为0.6(0.3- 1.1)和0.8(0.5-1.4)。因此,他们在反应中看不到生物学梯度。但是,许多农药的高暴露频率(例如73.8%的2,4-D暴露)意味着低草甘膦暴露的受试者很可能暴露于可能诱发非霍奇金淋巴瘤(NHL)的其他制剂;这可能会降低较高暴露类别中的RR,因为这会使低暴露参照人群中的RR膨胀。
Eriksson et al. (2008)[46]和McDuffie et al. (2001)[50]对每年的暴露强度有一致的结果(每年≤2天,OR = 1.0;每年≤10天,OR = 1.69;每年> 2天,OR = 2.12;每年> 10天年,或= 2.26)。不可能解决这三项研究之间的其余差异,也很难说一个研究对这个问题的重视程度超过任何其他研究。这些研究使用不同的暴露量度或自暴露以来的时间,针对不同的人群进行,并且具有不同的统计能力来检测趋势。
在啮齿动物致癌性研究中,有明确的证据表明存在生物梯度。
总的来说,有人支持存在生物学梯度的流行病学数据,因此从Bradford-Hill评估的这一方面提供了支持。
时间关系(Temporal Relationship)
必须暴露先于癌症,否则流行病学研究是无用的。 在这种情况下,很明显暴露是在非霍奇金淋巴瘤(NHL)发作之前发生的。满足了在数据中支持草甘膦和NHL之间因果关联时间关系的需求。
特异性(Specificity)
还有其他引起非霍奇金淋巴瘤(NHL)的原因[218-221],因此这组癌症不是草甘膦特有的。 对特有性几乎没有支持。
连贯性(Coherence)
接触草甘膦的人可以将其吸收到人体中,在血液和尿液中都可以检测到该化合物[56, 222-226]。 在实验动物中,对草甘膦和草甘膦化合物的吸收,分布和消除进行了研究[140, 227],结果表明草甘膦进入动物体内,分布到许多器官并在尿液中被消除。动物癌症研究清楚地表明,哺乳动物中的草甘膦可以具有毒性作用。
长期以来,小鼠模型一直是人类理解和研发治疗多种疾病药物的(人体的)替代物。对于在人类中看到的淋巴样肿瘤也是如此。 30多年来,已经研究并评估了小鼠模型作为非霍奇金淋巴瘤(NHL)的替代物[228-232]。 这些出版物和有关人类和小鼠的分类系统表明,人类和小鼠的疾病之间有着密切的联系。
因此,CD-1小鼠中恶性淋巴瘤的风险增加,瑞士小鼠中这些肿瘤的边缘性增加以及小鼠恶性淋巴瘤与人类非霍奇金淋巴瘤(NHL)之间的强烈相似性支持了连贯性。
在支持草甘膦和草甘膦制剂与非霍奇金淋巴瘤(NHL)因果关系的数据中,强烈支持连贯性。
人体实验证据
没有人类实验证据,因为有意将人类暴露于农药中,尤其是可能致癌的农药,这是不道德的,并且永远不会通过人类受试者咨询委员会的审查。
类似性
我不知道科学文献中有任何类似的化合物。 但是,这不是我有足够背景表达意见的领域。
总结
表18总结了希尔的因果关系各方面(Hill’s aspects of causality)的信息。对于这些数据,因果关系得到加强,因为现有的流行病学研究表明癌症与暴露之间存在一致的正相关性。这些研究没有显示出不同的反应,有些研究是肯定的,而另一些则是阴性,当一起分析时,它们也没有表现出任何异质性。而且,为回答希尔的问题,NHL和草甘膦暴露之间的关系已经由不同的人,在不同的地点,环境和时间观察到。
这些数据的因果关系得到了加强,因为当同时评估时,观察到的关联的强度在统计上是显着的,发现是单向的,并且结果不太可能是偶然的。即使没有一项单独的研究提供相对大的或精确的相对风险或比值比,但荟萃分析客观地表明,在这些研究中观察到的关联非常重要,并支持NHL与草甘膦之间的正关联。
动物的致癌性数据和遗传毒性和氧化应激的机理数据强烈支持生物学上的合理性。在解决生物学上的合理性时,通常要问的第一个问题是“您能否证明草甘膦会导致实验动物罹患癌症?”在这种情况下,该问题的答案显然是肯定的。草甘膦已被证明在两只老鼠和一只老鼠中引起癌症。草甘膦已被证明在两只老鼠和一只老鼠中引起癌症。草甘膦在雄性Wistar大鼠中引起肝细胞腺瘤,并在较小程度上在雄性Sprague-Dawley大鼠中引起雌性Wistar大鼠乳腺腺瘤和腺癌,在雄性Wistar大鼠中引起皮肤角膜癌,肾脏腺瘤和甲状腺C细胞腺瘤和癌。在雄性Sprague-Dawley大鼠中。草甘膦可引起雄性CD-1小鼠的血管肉瘤,肾脏肿瘤和恶性淋巴瘤,以及雌性CD-1小鼠的血管瘤,并可能引起雄性瑞士白化病小鼠的恶性淋巴瘤,肾腺瘤和雌性瑞士白化病小鼠的血管瘤。因此,草甘膦在哺乳动物中引起癌症。因此,从生物学上讲,仅草甘膦可以在哺乳动物中引起癌症。
通常要问的下一个问题是“草甘膦在实验动物中引起癌症的机制在人类中是否也起作用?”化学品引起人类和动物癌症的最佳机制是通过破坏DNA导致细胞突变,然后导致细胞失控复制并最终导致癌症。从现有的科学数据中绝对清楚,草甘膦和草甘膦制剂均具有遗传毒性。这已在暴露于草甘膦的人类,体外人类细胞,实验动物模型及其体外和体内细胞以及野生生物中得到充分证明。破坏DNA的一种方法是通过游离氧自由基的存在使细胞的抗氧化防御能力不堪重负。草甘膦会诱导这种氧化应激,为在人体中起作用的生物机制提供额外的支持。
表18:希尔的流行病学数据和相关科学的九个方面的总结性结论

总的来说,有人支持流行病学数据存在生物学梯度,因此从布拉德福德-希尔( Bradford-Hill)评估的这一方面提供了支持。 在评估至少其中一个问题的两个案例对照研究中,草甘膦ORs随首次接触的时间而增加,并随每年的使用强度而增加。
显然,与癌症发生前的暴露有适当的时间关系。
人类中的证据是连贯的。 人类中的基本发现与草甘膦吸收、分布和消除的动物证据相吻合。 同样,在小鼠中看到的一种肿瘤与非霍金斯淋巴瘤(NHL)具有几乎相同的病因。
非霍金斯淋巴瘤(NHL)并非是专门针对草甘膦的暴露。在人类中没有实验证据,在研究人员寻找具有相似毒性的类似化合物时,我也没有找到任何参考。
Hill (1965)[36]问道:还有没有其他方法可以解释我们面前的事实,是否有更平等或更多的答案的其他比因果关系?”没有比因果关系更好的方法来解释草甘膦与人类非霍金斯淋巴瘤(NHL)升高有关的科学证据。
在我看来,草甘膦可能引起非霍金斯淋巴瘤(NHL),并且根据已有人类、动物和实验的证据,我断言在合理的科学确定性下,草甘膦引起NHL的可能性很高。
国际癌症研究机构(IARC)对草甘膦的评估
2015年3月,国际癌症研究机构(世界卫生组织的一个机构)召集了17名科学家(工作组),对草甘膦是否会导致人类癌症的科学证据进行评估。该小组包括了一位受邀的专家(本人)协助工作组(WG)进行科学研究,但不允许其参加有关最终结论的讨论或撰写文档的任何部分。工作组得出结论,草甘膦属于“可能对人类致癌(2A组)”类别[56]。
IARC的序言[30]指导工作组如何评估科学文献以确定某物是否有害。所有工作组均遵循这些准则,该过程已被全世界公认为是评估危害性文献的适当方法(例如,欧洲化学局引用IARC审查过程作为指导,然后使用与IARC完全相同的措辞来指导他们自己的危害评估过程[34]。
工作组检查了流行病学数据,并将其归类为“致癌性的有限证据”,其定义是指“已观察到暴露于该病原体与癌症之间存在阳性相关关系,认为因果关系是可信的,但是偶然、偏见或混淆不能以合理的信心排除。”这是对流行病学研究证据强度的准确而清晰的描述。
工作组检查了来自动物致癌性研究的证据,并将其归类为“充分的致癌性证据”,IARC将其定义为:“已确定该病原与恶性肿瘤发病率增加或良性和恶性肿瘤适当组合之间存在因果关系。(a)两种或两种以上动物的恶性肿瘤,或(b)对一种动物进行两种或多种独立的研究,是在不同时间或在不同实验室或以不同方案进行的。当恶性肿瘤在发生率、部位、肿瘤类型或发病年龄方面以不同寻常的程度发生时,或在肿瘤在多部位发现有很强的发现时,可以考虑对一个物种和性别进行的一项单独研究提供了充分的致癌性证据。”根据IARC审查时可获得的数据以及序言可以审查的研究的限制,此结论是正确和正确的。
对该工作组审查的主要批评之一是,工作组没有审查监管机构可用的所有动物致癌性数据,因此得出了关于动物癌数据的错误结论。在这篇综述中,我评估了所有草甘膦评价机构共同提到的所有19种动物致癌性实验。在可能的情况下,我已经分析了原始数据并使用了可靠的统计方法来测试暴露于草甘膦的动物的癌症发病率显着增加。我的结论是,工作组会称此数据为“足够的证据”,以支持他们的发现,尽管未审查本文分析的其他研究。尽管业界对这些研究保密,但业界保留的这些研究中没有任何内容会改变工作组的结论。
关于机制性数据,国际癌症研究机构(IARC)工作组审查了与我审查的数据相同的数据,但在可能的情况下,我还评估了支持监管决策的专有数据。在可能的情况下,我重新分析了数据,以确保所呈现的结果是准确的。 IARC工作组使用其序言中列出的指导原则,宣布强烈支持基因毒性和氧化应激的生物学机制。正如我在此处所示,即使有行业研究的专有证据,这两种机制也得到了大力支持。因此,IARC工作组得出了正确的结论。
为了确定化合物的最终分类,国际癌症研究机构(IARC)的前言提供了有关如何使用这三个领域的分类的指南。如果人类的数据是“有限的”,而动物致癌性研究的数据是“足够的”,则讨论应从2A类开始,即“该物质可能对人类致癌”。然后,考虑到数据集的整体质量,来自机理研究的证据的强度以及需要考虑的任何其他科学问题,工作组将确定数据是否可用于不同类别。在这种情况下,工作组认为2A是正确的类别,我仍然认为证据支持这一发现。
美国环保署(EPA)对草甘膦的评估
与国际癌症研究机构(IARC)一样,环保署(EPA)在评估科学文献并确定某种化学物质的潜在致癌性时也有需要遵循的准则。 这些准则已经制定了多年,并以我本人和许多其他科学家提供给环保署(EPA)的可靠科学指导为基础。 对于草甘膦的评估,环保署(EPA)没有遵循他们自己的准则,也没有遵循健全的科学实践。 该意见与环保署(EPA)联邦杀虫剂、杀真菌剂与杀鼠剂法(FIFRA)科学咨询小组所做的审查一致[54]。 此外,环保署(EPA)未能找到所有相关的动物癌症研究,并曲解了其中的一些研究。 环保署(EPA)评价的主要问题是:
1,误解流行病学证据,将偏见的可能性和混淆的可能性与真实的偏见和真实的混淆相混淆,使他们几乎不重视病例对照研究,而仅倾向于某一项队列研究;
2,误解荟萃分析的结果;
3,在动物致癌性研究分析中未能正确使用历史对照;宣布一项重大发现不是由该化合物引起的,只要它在历史控制范围内;
4,未能分析行业提交所有研究中的所有肿瘤,依赖于业界提交的研究必定正确完成;
5,未能遵循什么构成阳性结果的指导原则,在没有相应的成对比较也很重要的情况下,无视重大趋势检验;
6,无视明显不超过动物最大剂量的阳性结果而损害研究的完整性;
7,对研究中的总体假阳性率使用不合理的论点,而未能对此问题进行实际分析;
8,未能认识到相似研究中的相似发现并未能进行汇总分析以确定一项研究中的阴性影响是否抵消了另一项研究中的阳性影响;
9,对公开发表文献研究很少重视,几乎完全依赖行业提供的研究,这些研究既没有质量也没有经过同行评审,更重要的是在某些情况下是对研究结果的解释(而非研究得出的结果);和
10,比较不同物种和品系的动物癌症研究和机理研究的结果时,很少考虑任何一项研究中的独特发现以及多项研究中的一致发现。
对欧洲食品安全局(EFSA)[89]和欧洲化学局(EuropeanChemicalAgency)[233]所做的评估的评论也与此类似。 随函附上我对这些机构进行的风险评估的详细评论。其他科学家对于我对美国环保署(EPA)的评论也有评论,我也在EPA关于草甘膦的档案中回应了这些评论。 这些也包含在附件中。

Dr.ChristopherJ.Portier(克里斯托夫 J. 帕特尔博士)
引用参考文献:(略)【注:可以访问下述链接查阅原文】
Christopher J. Portier, Ph.D., Expert Report, Case 3:16-md-02741-VC
Document 654-17 Filed 10/28/17
Christopher J. Portier, Ph.D.,专家报告,案件3:16-md-02741-VC
文件654-17,注册日期:2017年10月28日
https://usrtk.org/wp-content/uploads/2017/10/Chris-Portier-expert-report.pdf


 红歌会网 SZHGH.COM
红歌会网 SZHGH.COM


